Volume 10, No.1 Pages 24 -29
2. 最近の研究から/FROM LATEST RESEARCH
多孔性配位高分子のナノ細孔に吸着した水素分子の直接観測
Direct observation of hydrogen molecules adsorbed in a microporous coordination polymer
[1]大阪女子大学 理学部 Department of Environmental Sciences, Osaka Women’s University、[2](財)高輝度光科学研究センター 利用研究促進部門Ⅰ/CREST (JST) Materials Science Division, JASRI / CREST、[3]京都大学大学院 工学研究科 Department of Synthetic Chemistry and Biological Chemistry, Kyoto University、[4](財)高輝度光科学研究センター 利用研究促進部門Ⅰ/CREST (JST)、Materials Science Division, JASRI / CREST、[5]岡山大学 理学部 Department of Physics, Okayama University、[6]名古屋大学大学院 工学研究科 Department of Applied Physics, Nagoya University
- Abstract
- Hydrogen storage is one of the most important technologies, which is indispensable for the establishment of clean hydrogen energy system. Adsorption of H2 molecules in the metal-organic porous materials is one of the most promising candidates to store and release H2 molecules efficiently. To develop a rational synthetic strategy for novel metal-organic porous materials as hydrogen storages, the elucidation of the intermolecular interaction between H2 molecules and pore walls is essential and the fundamental structural characteristics of H2 molecules are required. Although the weakest X-ray scattering amplitude of hydrogen made it difficult to determine the structure, we have succeeded in direct observation of H2 molecules adsorbed in the nano-channels of the metal-organic porous material by in-situ synchrotron powder diffraction experiment of gas adsorption and MEM(maximum entropy method)/Rietveld analysis. The result could give us promising guidelines for designing hydrogen gas storage materials.
はじめに
水素は次世代のエネルギーシステムにおいて大変注目されている元素である。水素をエネルギーとして利用する利点はいくつかあるが、特に注目される点は、1)燃焼においてできる生成物が水であり、CO2や窒素酸化物などの有害汚染物質を排出しないので、環境負荷が少ないクリーンなエネルギーシステムができる。2)水素は私たちの身の回りにほとんど無尽蔵に存在し、資源的制限がない。という二点であろう。このような点から水素エネルギーへの期待は大変大きく、最近では燃料電池などの燃料としても利用されている。水素は電気エネルギーに比べると比較的容易に貯蔵が可能であり、その利用技術において、水素を大量にかつ効率的に貯蔵する技術が求められている。水素を貯蔵する方法には、ガスボンベに充填する、液体状態で貯蔵する、など色々な方法があるが、例えばボンベの場合、簡単に貯蔵ができる半面、15MPa程度の高圧で充填するため、ボンベ自身の強度が必要となり重量が大きくなってしまうというデメリットがある。また、液体水素は体積密度が大きいが、液化にかかるコストが大きい、などそれぞれ一長一短がある。一方で水素吸蔵合金に見られるように水素を物質に吸収させて貯蔵することができる。水素貯蔵材料としては、水素を大量にかつ効率的に貯蔵することが必要であるが、水素をよく吸収するだけでなく、容易に放出できることも重要である。水素貯蔵材料としてこれまで水素吸蔵合金や金属水素化物、カーボンナノチューブなどの炭素系材料など実に様々な物質が研究されてきたが、その中でも多孔性配位高分子は新しい材料として最近注目を集めている。
多孔性配位高分子[1, 2][1]S. Kitagawa, R. Kitaura and S. Noro : Angew. Chem. Int. Ed., 43 (2004) 2334.
[2]M. Eddaoudi et al. : Acc. Chem. Res. 34 (2001) 319.は、金属イオンと架橋有機分子の配位結合により、ブロックを積み上げるようにして作られたナノスケールの極めて均一な細孔構造を持つ。その細孔表面積は4000m2g-1を超えるものもあり、大変優れたガス吸着特性を示す。金属原子と有機分子の組み合わせを変えることによって、様々な大きさ・形状のナノ細孔を自在にデザインすることができる。また、化学合成が室温、1気圧下で行えることから産業化も比較的容易であり、新しい水素貯蔵材料として期待されている。
近年、多孔性配位高分子の研究は急速に進んでいて、ごく最近にも優れた水素吸着能をもつ物質の合成が多数報告されている[3-6][3]G. Férey et al. : Chem.Commum. 24 (2003) 2976.
[4]D. N. Dybtsev, H. Chun and K. Kim : Angew. Chem. Int. Ed. 43 (2004) 5033.
[5]L. Pan et al. : J. Am. Chem. Soc. 126 (2004) 1308.
[6]J. L. C. Rowsell, A. R. Millward, K. S. Park and O. M. Yaghi : J. Am. Chem. Soc. 126 (2004) 5666.。しかし、これまで大変多くの報告がありながら、吸着水素分子がナノ細孔内のどのような位置に吸着しているかは全く明らかにされていなかった。設計性に富んだこの物質の新規合成を進めていく上で、水素分子とナノ細孔との相互作用を理解することは大変重要である。そのために水素分子のナノ細孔内での振る舞いを知る基本的な構造情報は欠かせないものである。水素はX線散乱能が小さいため、これまでX線を使った水素の位置決定は難しいとされてきた。ましてや、細孔内に吸着した気体分子の水素を観測することはこれまで全く例がなかった。
私たちは、これまでの多孔性配位高分子へのガス吸着の研究において、高輝度放射光とマキシマムエントロピー法(MEM)という電子密度解析法を用いて、ナノ細孔内に物理吸着した酸素分子の整列構造を世界で初めて明らかにした[7][7]R. Kitaura et al. : Science 298 (2002) 2358.。その結果から、細孔内でのバルクとは異なった磁気的性質や吸着現象を理解する基本的な構造情報を得ることができた。MEMはX線回折データを統計的に処理し、フーリエ級数の打ち切り効果の影響が少ない高分解能の電子密度分布を得ることができる方法なので、X線散乱能の小さい水素でも高輝度放射光を用いて高精度の回折データを得ることができれば、観測は十分に可能であると考えられる。放射光とMEMを組み合わせた手法によりX線で水素を観測する試みは最近いろいろな分野でなされている。例えば、金属水素化物MgH2では、吸蔵された水素原子の位置だけでなく、水素原子とMg原子との間の化学結合までもクリアに観測されている[8][8]T. Noritake et al. : Appl. Phys. Lett. 81 (2002) 2008.。タンパク質においても水素の役割は大変重要であり、今や炭素や酸素などの原子配置だけでなく水素の位置や結合状態に大きな関心が持たれている。ごく最近には専用スーパーコンピュータを用いた解析によりタンパク質中の水素のより精密な構造解析が試みられている[9][9]西堀英治、有本将規、坂田誠、吾郷日出夫、宮野雅司 : 日本結晶学会2004年度年会講演要旨。。
今回、私たちはSPring-8の高輝度放射光とMEM電子密度解析を用いて、世界で初めてナノ細孔に吸着した水素分子を観測することに成功した[10][10]Y. Kubota et al. : Angew. Chem. Int. Ed. 44 (2005) in press.。その研究成果について紹介する。
ガス吸着状態の放射光粉末回折実験
今回用いた試料は銅配位高分子[Cu2(pzdc)2(pyz)]n
(pzdc=ピラジン-2, 3-ジカルボン酸、pyz=ピラジン)である[11][11]M. Kondo et al. : Angew. Chem. Int. Ed. 38 (1999) 140.。pzdcの2次元シートとそれをつなぐピラジン分子で構成されるいわゆるピラードレイヤータイプの構造をもち、私たちはこの物質を通称CPL-1(coordination polymer 1 with pillared layer structure)と呼んでいる。CPL-1の基本構造は単結晶X線回折により解かれていて(図1)、大きさが4×6Åの一次元ナノ細孔を持つ。
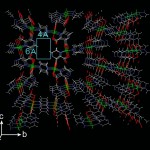
図1 CPL-1の結晶構造
空間群はP21/c、格子定数はa=4.693(3)Å、b=19.849(2)Å、c=11.096(2)Å、β=96.90(2)°である。合成時に細孔に含まれている水分子は省略している。
ガス吸着状態での放射光粉末回折データのその場測定はSPring-8の粉末結晶構造解析ビームラインBL02B2において、大型デバイシェラーカメラ[12][12]M. Takata et al. : Adv. in X-ray Anal. 45 (2002) 377.にガス吸着実験用システムを組み合わせて行った。イメージングプレートを検出器としたデバイシェラー法では、全ての回折線が同時測定されるので、非常に統計精度が高いデータが得られ、また測定条件が一定しているのでその場測定には適していると考えられる。図2に試料周辺の写真を示す。粉末試料は内径0.4mmのガラスキャピラリに充填し、ガス導入用試料ホルダーに取り付けた。水素ガスは試料ホルダーに接続したステンレス管を通して導入される。試料温度は窒素ガス吹き付け型低温装置により制御した。このシステムでは通常とほとんど同じ状態で簡便にガス吸着のその場測定が行える。入射X線の波長は0.8Åとした。はじめに383Kで15分間試料を加熱し、細孔内の水分子を取り除いた。水分子の脱着は回折パターンを見て確認した。その後、温度を室温に下げて水素ガスをほぼ常圧102kPa導入した。そして、ガス導入バルブを閉じ、水素ガス圧を一定に保ったまま温度を順次下げていき、水素を吸着させた。

図2 BL02B2におけるガス吸着実験システムの試料周りの写真
図3は水素ガスを導入したCPL-1の粉末回折パターンの温度変化である。200Kの回折パターンは細孔内に何も入っていない空のCPL-1と同じ回折パターンになっている。温度を下げていくと、110Kから90Kにかけて、ピーク位置のシフトと回折強度の変化が認められた。図の一番下には参考として、水素ガスを入れない空のCPL-1の90Kの回折データを描いてあり、水素ガスを導入した場合には90Kで何らかの構造変化が起こっていることは明らかである。図4にこれらの回折パターンから得た格子定数と単位格子体積の温度変化を示す。a軸は一次元細孔の方向である。110Kあたりからa軸以外の格子定数および単位格子体積が増え始め、90Kで大きく増加している。以上のデータは90KにおいてCPL-1の細孔内に水素が吸着されたことを示していると考えられる。90Kにおける水素ガス吸着量は吸着等温線の測定データより、銅原子1個あたり0.3個と見積もられた。以後の解析では吸着水素原子の占有率を0.3に固定した。
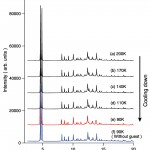
図3 水素ガスを導入したCPL-1の粉末回折データの温度変化
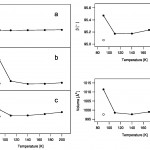
図4 水素ガスを導入したCPL-1の格子定数と単位格子体積の温度変化
白丸は空のCPL-1の値を示している。
MEM/Rietveld法による電子密度分布解析
電子密度分布解析はMEM/Rietveld法[13][13]M. Takata, E. Nishibori and M. Sakata : Z. Kristallogr. 216 (2001) 71.を用いて行った。吸着ガス分子の構造解析では始めに分子が細孔内のどのような位置にあるかはほとんどわからない。従来の解析法では色々な位置、向きに分子を置いた多数の構造モデルに対してRietveld解析を行い、最も信頼度因子が小さくなる構造モデルを採用するという方法が取られる。しかし、そのような場合、膨大な構造モデルを試す必要があり、解析は困難を極める。特に吸着分子の大きさが細孔の大きさに対してずっと小さい場合は難しいと思われる。しかし、与えた実験データに合った電子密度分布を非常にクリアにイメージングできるというMEMの特性を積極的に利用すれば、構造モデルの構築を合理的に行うことができる。この方法は金属内包フラーレン[14-15][14]M. Takata et al. : Nature 377 (1995) 46.
[15]C. Wang et al. : Nature 408 (2000) 426.や吸着酸素分子[7][7]R. Kitaura et al. : Science 298 (2002) 2358.の構造解析において威力を発揮した。
水素を含んだCPL-1の粉末回折パターンに対し、最初のRietveld解析では、吸着水素分子を仮定しない空のCPL-1の構造モデルを用いた。粉末回折パターンのプロファイルに基づく信頼度因子RWPとBragg反射強度に基づく信頼度因子RIの値はそれぞれRWP=2.47%、RI=3.39%であった。通常のRietveld解析としては十分なフィッティングがされている。この解析結果を利用して観測回折強度を個々の回折線に振り分け、積分反射強度を得た。積分反射強度から得られた結晶構造因子とその誤差を使ってMEMにより電子密度のイメージングを行った。MEMの計算はプログラムENIGMA[16][16]H. Tanaka et al. : J. Appl. Crystallogr. 35 (2002) 282.を用いて行い、計算において与えた単位格子内の総電子数は水素分子の占有率を考慮して538.4個とした。解析にはsinθ/λ≦0.680Å-1のデータを用いた。MEM解析の結晶構造因子に基づく信頼度因子RFは2.24%であった。構造モデルに吸着水素分子を仮定していないにも関わらず、得られたMEM電子密度分布には細孔内に電子密度のピークが見られた。このピークを吸着水素分子によるものと考え、ピーク位置に水素分子を置いたモデルを新たな構造モデルとした。Rietveld解析およびMEM解析の最終的な信頼度因子はそれぞれRWP=2.45%、RI=3.33%、RF=1.86%となり、わずかではあるが改善した。また、参照として水素ガスを導入しない空のCPL-1の90Kのデータも同様に解析した。信頼度因子はそれぞれRWP=2.21%、RI=3.89%、RF=2.50%となった。
ナノ細孔への水素分子の吸着構造
図5にCPL-1のMEM電子密度分布を示す。図5(a)に示す水素を導入しない空のCPL-1の電子密度分布には細孔構造のみがクリアに観察され、非常に低い電子密度レベルで見ても細孔内には何も電子分布は観察されない。一方、図5(b)の水素ガスを導入したCPL-1の電子密度分布には細孔構造とともに細孔内に青く色をつけて示した少し細長い形をした小さな電子密度のピークがイメージングされていることがわかる。この電子密度ピークの周りの電子数を数えると0.6(1)個であった。これは吸着等温線から見積もった水素の占有率の値と対応する。したがって、この電子密度のピークは吸着水素分子のものであると判断した。水素分子は細孔の方向に対してジグザグに整列している。これは酸素分子の場合、ダイマーを形成しながら整列している様子[7][7]R. Kitaura et al. : Science 298 (2002) 2358.とは異なり、水素分子を引き付ける吸着サイトが存在することをうかがわせる。そして、水素分子はCPL-1の細孔壁と化学結合を作るのではなく、細孔壁とは独立して存在していることがわかる。電子数も考え合わせると、水素分子は弱い相互作用によっていわゆる物理吸着されていて、出し入れが容易な状態で吸着されていると考えられる。水素の放出が比較的容易に行えるのは水素貯蔵物質としての配位高分子の特徴であると言えよう。

図5 CPL-1のMEM電子密度分布
(a) 水素ガスを導入しない場合 (b)、(c) 水素ガスを導入した場合等電子密度のレベルは(a)、(b)が0.11eÅ-3、(c)が0.8cÅ-3である。(c)には原子モデルを重ねて描いてある。
この解析で得られた水素分子の位置や向きは統計的な解析により得られた平均の値を示している。つまり、物理吸着した水素分子は90Kにおいても大きく熱振動していると考えられる。実際に吸着水素分子の電子密度はCPL-1骨格を構成するピラジン分子の水素原子の分布(図5(c))に比べて非常にブロードになっている。このことを踏まえた上で、水素分子の位置を詳しく見るために、ひとつの細孔部分の電子密度分布を拡大して見る(図6)。水素分子は細孔の中央ではなく少し細孔壁に寄った位置に存在していることがわかる。4×6Åの細孔の大きさは水素分子の大きさに比べて十分大きく、水素分子が四角形の細孔の角の方向に引き付けられているように見える。図6にはCPL-1骨格を構成する原子のモデルを電子密度分布に重ねて描いてあるが、吸着水素分子は細孔の角に位置する赤で色をつけた酸素原子の近くに存在することがわかった。CPL-1骨格に酸素原子はいくつか存在するが、この酸素原子は銅原子と結合したカルボン酸に属する原子であり、水素分子はCu-OOCのCu−Oユニットに引き寄せられているように見える。非常に興味深いことは、これまで報告されている優れた水素吸着能を持つ多孔性配位高分子[3-6][3]G. Férey et al. : Chem.Commum. 24 (2003) 2976.
[4]D. N. Dybtsev, H. Chun and K. Kim : Angew. Chem. Int. Ed. 43 (2004) 5033.
[5]L. Pan et al. : J. Am. Chem. Soc. 126 (2004) 1308.
[6]J. L. C. Rowsell, A. R. Millward, K. S. Park and O. M. Yaghi : J. Am. Chem. Soc. 126 (2004) 5666.の多くは、金属(M)−酸素のユニットを細孔の角付近に有するという点である。この共通したM−Oユニットは何らかの水素分子を誘引する効果を持つのではないかと考えられるが、吸着現象においてどの程度の寄与があるのかについては今後の研究課題である。
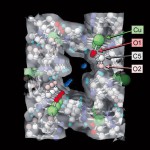
図6 CPL-1の細孔部分のMEM電子密度分布等電子密度のレベルは0.11eÅ-3である。CPL-1骨格の原子モデルを重ねて描いてある。
もう一点注目すべき点は細孔壁の形である。CPL-1の構造モデルを示したときに4×6Åの四角形の細孔と書いたが、図6を見てわかるとおり細孔壁面は凹凸を持っている。水素分子は細孔壁のくぼみの部分にすっぽりはまるように位置していることがわかる。つまり、CPL-1においては細孔のくぼみの大きさが水素分子の大きさと非常にうまくフィットしている。この配置では水素分子は細孔壁からの引力を大変効果的に受けていると考えられる。
おわりに
以上に示してきたように、今回私たちはナノ細孔に吸着した水素分子の観測に成功し、その詳細な構造情報を得ることができた。その結果から次のようなことが示唆される。1)金属原子−酸素原子の構造ユニットが何らかの水素分子を誘引する効果を持つ。2)細孔壁の形状が水素分子とうまくフィットすることが吸着に効果的である。本研究では水素の吸着量がかなり少ない状態で調べたが、そのおかげで私たちは吸着初期段階の構造情報を得ることができた。つまり、水素分子が始めに細孔のどこに吸着されるかという大変重要な情報を始めて明らかにすることができた。これは水素貯蔵材料としての多孔性配位高分子を設計していく上での正に指針を与え得るものと考えられる。今後、その設計指針に基づいた高性能水素貯蔵物質の開発が期待され、将来の水素エネルギー利用技術の発展に貢献できるものと考えられる。
本研究は京都大学大学院工学研究科北浦良博士(現:豊田中央研究所)、松田亮太郎氏との共同研究である。本研究は文部科学省ナノテクノロジー支援プロジェクトおよび科学研究費補助金の支援を受け、科学技術振興事業団の戦略的創造研究推進事業の一環として実施された。MEM解析のプログラムENIGMAについては島根大学総合理工学部の田中宏志助教授にご協力いただいた。
参考文献
[1]S.Kitagawa, R.Kitaura and S.Noro : Angew.Chem.Int.Ed., 43(2004)2334.
[2]M.Eddaoudi et al. : Acc.Chem.Res.34(2001)319.
[3]G.Férey et al. : Chem.Commum.24(2003)2976.
[4]D.N.Dybtsev, H.Chun and K.Kim : Angew.Chem.Int.Ed.43(2004)5033.
[5]L.Pan et al. : J.Am.Chem.Soc.126(2004)1308.
[6]J.L.C.Rowsell, A.R.Millward, K.S.Park and O.M.Yaghi : J.Am.Chem.Soc.126(2004)5666.
[7]R.Kitaura et al. : Science 298(2002)2358.
[8]T.Noritake et al. : Appl.Phys.Lett.81(2002)2008.
[9]西堀英治、有本将規、坂田誠、吾郷日出夫、宮野雅司 : 日本結晶学会2004年度年会講演要旨。
[10]Y.Kubota et al. : Angew.Chem.Int.Ed.44(2005)in press.
[11]M.Kondo et al. : Angew.Chem.Int.Ed.38(1999)140.
[12]M.Takata et al. : Adv.in X-ray Anal.45(2002)377.
[13]M.Takata, E.Nishibori and M.Sakata : Z.Kristallogr.216(2001)71.
[14]M.Takata et al. : Nature 377(1995)46.
[15]C.Wang et al. : Nature 408(2000)426.
[16]H.Tanaka et al. : J.Appl.Crystallogr.35(2002)282.
久保田 佳基 KUBOTA Yoshiki
大阪女子大学 理学部 環境理学科
〒590-0035 大阪府堺市大仙町2-1
TEL:072-222-4811 内線4343 FAX:072-222-4791
e-mail:kubotay@center.osaka-wu.ac.jp
高田 昌樹 TAKATA Masaki
高輝度光科学研究センター 利用研究促進部門Ⅰ,CREST(JST)
〒679-5198 兵庫県佐用郡三日月町光都1-1-1
TEL:0791-58-0946 FAX:0791-58-0946
e-mail:takatama@spring8.or.jp
北川 進 KITAGAWA Susumu
京都大学大学院 工学研究科合成・生物化学専攻
〒615-8510 京都市西京区京都大学桂
TEL:075-383-2733 FAX:075-383-2732
e-mail:kitagawa@sbchem.kyoto-u.ac.jp
加藤 健一 KATO Kenichi
高輝度光科学研究センター 利用研究促進部門Ⅰ,CREST(JST)
〒679-5198 兵庫県佐用郡三日月町光都1-1-1
TEL:0791-58-0802 内線3476 FAX:0791-58-0830
e-mail:katok@spring8.or.jp
小林 達生 KOBAYASHI Tatsuo
岡山大学 理学部 物理学科
〒700-8530 岡山市津島中3-1-1
TEL:086-251-7826 FAX:086-251-7830
e-mail:kobayashi@psun.phys.okayama-u.ac.jp
坂田 誠 SAKATA Makoto
名古屋大学大学院 工学研究科 マテリアル理工学専攻
〒464-8603 名古屋市千種区不老町
TEL:052-789-4453 FAX:052-789-3724
e-mail:sakata@cc.nagoya-u.ac.jp
(実験責任者 北川 進)
使用ビームライン:BL02B2
シフト数:9シフト(2004年11月10日〜12日、
2004年12月3日〜4日)
課題番号:2003B0461-ND1b-np-Na
(実験責任者 北川 進)
使用ビームライン:BL02B2
シフト数:12シフト(2003年10月29日〜31日、
2003年12月9日〜11日)
課題番号:2003A0371-ND1-np
(実験責任者 北川 進)
使用ビームライン:BL02B2
シフト数:12シフト(2003年3月15日〜17日、
2003年6月9日〜11日)








