Volume 16, No.1 Pages 3 - 9
1.最近の研究から/FROM LATEST RESEARCH
リン酸化オリゴ糖カルシウム(POs-Ca)による初期むし歯のエナメル質の再結晶化の検証
Investigation of the Recrystallization of Early Carious Enamel with Phosphoryl Oligosaccharides of Calcium
江崎グリコ(株) 健康科学研究所 Institute of Health Sciences, Ezaki Glico Co., Ltd.
- Abstract
- 歯の表面を覆うエナメル質はカルシウムを含む化合物であるハイドロキシアパタイト(HAp)結晶が規則正しく並んだ構造を形成し、丈夫な性質を維持している。しかし、食後に発生する酸でエナメル質表層下のHApは容易に溶け出し(脱灰)、初期むし歯(初期う蝕)を形成する。一方、リン酸化オリゴ糖カルシウムとそれを配合したガムは水溶性のカルシウムを唾液に供給する。これまでの研究から、リン酸化オリゴ糖カルシウム存在下では効率よくカルシウムの回復(再石灰化)が進むことがわかっていたが、回復したカルシウムがHAp結晶構造を正しく構成できるかどうかの詳細は不明確であった。われわれはSPring-8 BL40XUのマイクロX線を用いた回折法により、非破壊的にエナメル質表層の局所的な結晶量と配向性を調べる方法を確立した。そして実際に初期むし歯の再石灰化が起こった部分で、元の歯と同じ配向をもったHAp結晶が増加し、健全な状態に戻ったことを確認した。
はじめに
甘い物を食べるとむし歯になる — 子供の頃に親にそう言い聞かされた方は多いだろう。しかし、「ガムを食べてむし歯にならないようにする」と言ったらどうであろう。われわれは一見矛盾するように思えるこの発想を実現している。ガムの効果・効能の研究の一環として自社製の新しいカルシウム素材であるリン酸化オリゴ糖カルシウムと、それを配合したガムの初期むし歯予防効果について最先端の放射光施設であるSPring-8で2007年より研究を行い、光栄にも2010年度の第8回「ひょうごSPring-8賞」をいただいた。本稿では今回の研究対象であるむし歯の背景と研究内容について概説したい。
1.人類とむし歯
むし歯は有史以来、糖類を常に食べるようになった人類を悩ませ続けてきた病気である。現在ではむし歯は感染症であることが分かっており、その原因菌と発症メカニズムも明らかになっている。つまり口の中の細菌(ミュータンス連鎖球菌など)が食べ物に含まれる糖を餌に酸を発生させ、その酸が歯を溶かすことで起こる。しかし、原因菌がわかっていながら未だその撲滅にはいたっていない。むし歯にならないためには専ら日常的な予防をすることが必要なのである。
むし歯は直接死には至る病ではないが、食べ物が食べにくくなるなどQOL(quality of life)を著しく低下させるだけでなく、消化や口内環境の悪化によって全身の健康に影響を及ぼしうる。また、歯科治療に係る医療費に目を向けると、現在は全疾病のうちでも悪性新生物(がん)とほぼ並んでNo.1の地位を占めている。その全てがむし歯治療に係る費用というわけではないが、想像以上にむし歯は重大な現代病といえる。それを受けて、厚生労働省は2000年より「21世紀における国民健康づくり運動」の一環として「80歳までに20本の歯を保つ」ための取り組み「8020(ハチマルニイマル)運動」を展開し、着実に成果を上げている。
2.歯の構造と初期むし歯(初期う蝕)
本研究で扱っている初期むし歯(初期う蝕)とは、むし歯(う蝕)の初期段階のことで、実質欠損(視覚的に穴のあいている状態)ではない。歯科検診では経過観察が必要な要注意歯(CO(シーオー))として扱われるものの、必ずしも外科的な治療が必要な疾病ではない。初期むし歯がどのように形成されるかを見る前に、歯がどのような構造から成っているかを述べたい。
歯は外側をエナメル質という人体で最も硬い構造(モース硬度6−7、石英と同じ程度の硬さ)で覆われている(図1)。エナメル質は96%が無機質であり、ほとんどがカルシウムとリン酸、水酸化物イオンからなるハイドロキシアパタイト(Ca10(PO4)6(OH)2、HApと呼ぶ)の結晶である。HAp結晶は、歯の表面に対して垂直方向に並び、直径3−5 µmのエナメル小柱(crystallite)を形成している。さらにエナメル小柱が各生物に特有の様式で規則正しく並んでいる。このように一様に並んだHAp結晶は、そのc面を歯の表面に露出することになる。HApのc面はa面に比べて表面エネルギーが低く[1][1] M. R. T. Filgueiras, D. Mkhonto and N. H. De Leeuw: J. Cryst. Growth 294 (2006) 60-68.酸に対して強く、そして硬い[2][2] S. Saber-Samandari and K. A. Gross: Acta Biomater. 5 (2009) 2206-2212.ため、乱雑に並んだ場合よりもエナメル質の耐酸性は高まっている。ちなみに骨もHApを含んでいるが、その割合は65%であり、残りはコラーゲンなどのタンパク質である。結晶の配向性もエナメル質に比べて低い。そのため、エナメル質より軟らかく、しなやかな構造になっている。
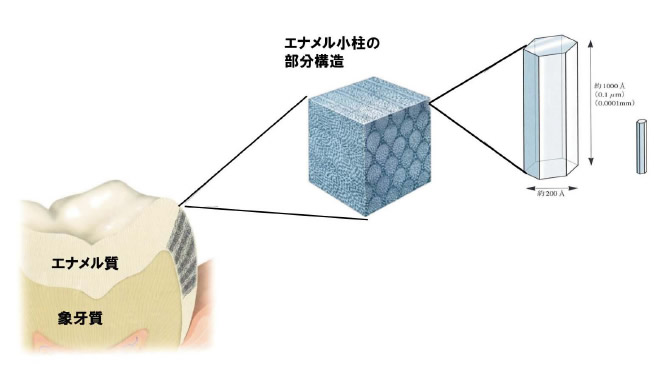
図1 歯とエナメル質の構造
(出典)「イラストでみるこれからのむし歯予防」花田信弘 監修 砂書房
HApは中性ではほとんど水に不溶であるが、pH5.5以下になると急速に溶解度が上がる。ほとんどの人の口の中にはミュータンス連鎖球菌などのう蝕原性細菌と呼ばれるバクテリアが棲みついている。う蝕原性細菌はショ糖を利用して酸を産生するとともに、歯の表面に付着するためのグルカンというねばねばした物質を産生する。こうして歯にプラーク(歯垢)が形成され、産生される酸によってエナメル質は局所的に溶け出してしまう。このときエナメル質では、カルシウム−リン酸の溶出と、外部からのカルシウム−リン酸供給のバランスによって、表層は保たれたまま表層付近から数百µmほど内側のHApが溶出されていく。これを表層下脱灰(図2)と呼んでいる。初期むし歯は表層下脱灰が続いている状態と定義することができる。

図2 エナメル質横断面のマイクロラジオグラフ表層下脱灰部領域(矢印)
3.初期むし歯の予防−初期むし歯に唾液を通じたカルシウム供給
初期むし歯はわれわれの日常生活の中では決して特殊な状態ではなく、日々の生活において歯のカルシウム−リン酸の溶出と再構成のバランスが崩れると容易に発生する。歯垢内は食事のたびに酸性に傾き、歯エナメル質からカルシウムイオンとリン酸イオンがわずかに溶け始める。人の歯は永久歯萌出以降生え変わったり伸びたりすることはないため、カルシウム−リン酸の溶出と再構成のバランスが崩れ、溶出が続く一方であれば、歯エナメル質に穴が開き、むし歯に至ってしまう。しかし実際には、エナメル質を健康に保つために唾液がカルシウムとリン酸を常に供給している。唾液はおよそ1−2 mMのカルシウムイオンと、2−23 mM(咀嚼で分泌される刺激唾液には3−4 mM)のリン酸イオン(厳密にはリン酸水素イオン、リン酸二水素イオンの状態が多い)のほか、重炭酸イオンなどを含みpH緩衝作用のあるほぼ中性の液体である。そのため、唾液は食べ物かすを洗い流すとともに酸性に傾いた歯垢内pHを中性に戻し、さらにエナメル質に失われたカルシウムとリン酸を供給する働きをもつ。
表層が残っている初期むし歯の状態では、唾液によって供給されたカルシウムとリン酸は再度エナメル質の構成要素として取り込まれ、元の状態に戻っていく(再石灰化)。しかし、脱灰が進んで表層が崩壊して歯に穴が開いてしまうと、唾液中にカルシウムとリン酸が存在していても物理的に穴がふさがることはない。すると、歯は不可逆的に蝕まれるようになり、放置すればやがて象牙質にまで穴が到達して、苦痛を伴ったむし歯として知覚されるようになる。表層が失われてしまえば、外科的な措置なくしてむし歯は治らないのである。したがって、健康な歯を維持していくためには初期むし歯の状態のときにいかに「脱灰<再石灰化」となるようにうまく唾液のカルシウムを高める口内環境を構築できるかが重要となる。
4.リン酸化オリゴ糖カルシウムの初期むし歯に対する有効性
リン酸化オリゴ糖カルシウムは、江崎グリコ(株)が独自に開発した機能性カルシウム素材である。元々はジャガイモ澱粉から糖を生成するときに不要とされていた画分から、リン酸化オリゴ糖と呼ぶ3−7個のグルコース単位からなる直鎖オリゴ糖に1ないし2個のリン酸基が結合した物質を分離した[3][3] H. Kamasaka, M. Uchida, K. Kusaka, K. Yoshikawa, K. Yamamoto et al.: Biosci. Biotechnol. Biochem. 59 (1995) 1412-1416.(図3)。負電荷をもつリン酸基がカルシウムイオンを安定化し、またオリゴ糖部分が高い親水性をもつことで、カルシウムイオンを水に溶けた状態に保つ作用がある。カルシウムとリン酸の化合物はほとんどが不溶性の塩を作ってしまうため、唾液にカルシウムをさらに外部から補給しようとしても、含まれるリン酸によって不溶化されてしまうことがあった。しかし、リン酸化オリゴ糖カルシウムは再石灰化に有効なカルシウムイオンを効果的に唾液へ供給できる素材であることがわかっている[4][4] H. Kamasaka, D. Inaba, K. Minami, S. Imai and M. Yonemitsu: J. Dent. Hlth. 52 (2002) 105-111.。また、リン酸化オリゴ糖はオリゴ糖でありながら、ミュータンス連鎖球菌に利用されないため、糖アルコール等の代替甘味料と同様にむし歯の原因とならないこと、またpHが極端に酸性になることを防ぐ緩衝作用があることも明らかとなり、むし歯予防に理想的な素材であることがわかってきた[5][5] H. Kamasaka, S. Imai, T. Nishimura, T. Kuriki and T. Nishizawa: J. Dent. Hlth. 52 (2002) 66-71.。
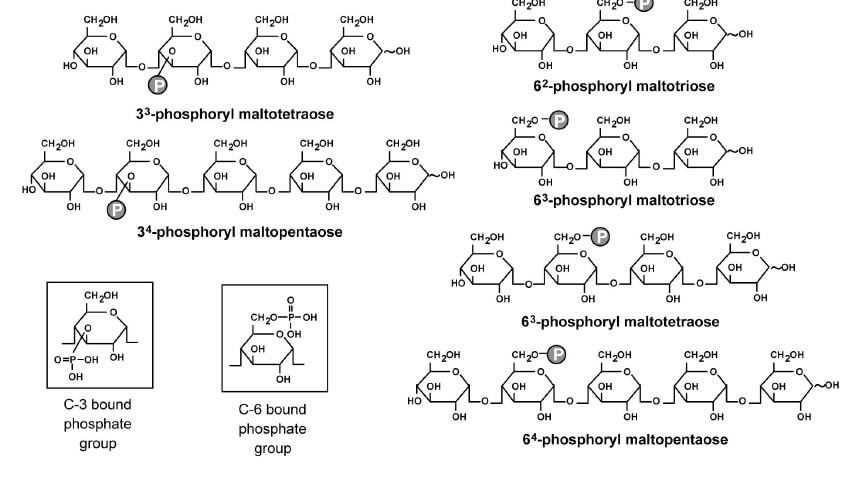
図3 リン酸化オリゴ糖の構造
リン酸基1つを有する主な画分(PO-1画分)に含まれるオリゴ糖を示した。
そこで、われわれはまずリン酸化オリゴ糖カルシウムが歯の再石灰化を促進するかどうかを歯科で一般的に用いられているX線透過法であるtransversal microradiography(TMR)法で検証した。歯からエナメル質部分を平滑にしてから切り出し、擬似的な歯表面とした。表面の一部をコートしたのち、これに口内での脱灰に相当する緩やかな酸処理を行うことで、表層下脱灰を形成させた。その後、さらに一部をコートして外液に触れないようにしてから、唾液と同量のカルシウムとリン酸を含む溶液(人工唾液)に浸した。これにより、最終的に何も処理していない領域(健全部、SOUND)、脱灰したままの領域(脱灰部、DEM)と再石灰化した領域(再石灰化部、REM)を同一の歯面に作り出した。これを歯面に垂直な方向に切りだし、厚さ150 µmの薄い切片とした。平行なX線を歯片に照射し、反対側に感光フィルムを置くことで歯の深さ方向のミネラル量をフィルムの濃淡として検出した(図4a)。撮影像を画像処理することで、ミネラルプロファイルが得られる。健全部に対して脱灰部で失われたミネラル量(ΔDEM)と脱灰部から再石灰化部にかけて回復したミネラル量(ΔREM)は各プロファイルの深さに対する積分値から求められる。(ΔDEM−ΔREM)/ΔDEM × 100をミネラル回復率と定義して、再石灰化の効率を評価した(図4b)。
人工唾液ではリン酸に対するカルシウムイオンの割合(Ca/P)が0.4程度と、カルシウムが相対的に少ない。そこにリン酸化オリゴ糖カルシウムを添加することで、Ca/P=1.67というHApに相当する比率にまで高めることにより、より効率よく再石灰化が進むことが確認された[4][4] H. Kamasaka, D. Inaba, K. Minami, S. Imai and M. Yonemitsu: J. Dent. Hlth. 52 (2002) 105-111.。また、リン酸化オリゴ糖カルシウムの代わりに塩化カルシウムをCa/P=1.67になるように加えても、再石灰化効率はリン酸化オリゴ糖カルシウム処理の場合に比べて低いことが明らかとなっている(図4c)。このことから、リン酸化オリゴ糖カルシウムが効率よく再石灰化を促進する物質であることが裏付けられた。
さらに、東京医科歯科大学(う蝕制御学講座 田上順次教授)の研究では、あらかじめ脱灰処理したエナメルブロックを埋め込んだ口腔内装置を被験者に装着してもらい、リン酸化オリゴ糖カルシウムを含むガムをかんだ場合と、リン酸化オリゴ糖カルシウムを含まないガムをかんだ場合で口内での再石灰化の違いが起こるかどうかが検討された。その結果、上記の人工唾液を用いた試験と同様にPOs-Caによって有意に再石灰化が促進されていることが明らかとなった[6][6] 田中美由紀、北迫勇一、二階堂徹、半場秀典、池田正臣他:日本歯科保存学雑誌 52 (2009) 534-542. 。したがって、臨床的にもPOs-Caは再石灰化促進作用を持つことが明らかとなった。

図4 TMRによるエナメル質のミネラル量の定量
(a)TMR像の例。(b)典型的なミネラルプロファイルとミネラル回復率の算出法。(c)リン酸化オリゴ糖カルシウム(POs-Ca)と塩化カルシウム(CaCl2)を再石灰化に用いたときの回復率比較。
5.再石灰化=「再結晶化」か?
従来用いられてきたTMR法では、脱灰・再石灰化により表層下のミネラル量変化を捉えられたが、エナメル質のHAp結晶の構造物の変化を捉えることはできなかった。例えば、常温・中性条件下でカルシウムイオンとリン酸イオンを水中で混合した場合には、直接HApが生じることはなく、まずアモルファスリン酸カルシウム(amorphous calcium phosphate、ACP)やリン酸オクタカルシウム(octacalcium phosphate、OCP)が生じる。一方でHAp結晶の土台がある表層下では、直接結晶成長によりHApの構造が再構築される可能性があった。これまで表層付近の結晶構造を分析する方法として、走査型電子顕微鏡(SEM)や透過型電子顕微鏡(TEM)を用いた方法がとられてきた。非常に微細な構造の定性的な議論はできる一方、サンプルに対して破壊的である上に、定量性を持ったデータは得ることができなかった。先に述べたように、HApの配向性はエナメル質の耐久性に関わる。そこで、歯の再石灰化だけではなく「再結晶化」というレベルまで追究することは、歯の健康維持に貢献できる商品であることを保証するために重要であるとわれわれは考え、再結晶化の検証を試みることとした。
6.SPring-8におけるエナメル質の再結晶化の検証[7,8][7] N. Yagi, N. Ohta, T. Matsuo, T. Tanaka, Y. Terada et al.: J. Synchrotron Rad. 16 (2009) 398-404.
[8] T. Tanaka, N. Yagi, T. Ohta, Y. Matsuo, Y. Terada et al.: Caries Res. 44 (2010) 253-259.
われわれは、まず粉末X線回折を用いてエナメル質の結晶構造の解析を試みた。表層から深さ方向の結晶構造変化を調べるために、表層から数十マイクロメートルごとにエナメル質を削り、得られた粉末をX線回折法で測定することで、OCPやACPではなくHApが再石灰化で生成されているかどうかを調べた。しかし、エナメル質の大部分を占めるHApはOCPやACPに比べてはるかに結晶性が高いため、強い回折強度をもつHApのピークが他者のピークを覆い隠してしまうという問題があった(なおACPとOCPの検出が困難であることは、現在用いているX線回折法にも当てはまる解決すべき問題のひとつである)。結局、サンプルを破壊することによって、i )元の配向性の情報、ii)深さ方向の細かい分布情報、iii)定量性の情報が失われてしまったため、有益な情報が得られなかった。しかし、この試みの過程で粉末X線回折をSPring-8 BL19B2で行ったことがきっかけとなり、今日のSPring-8の成果が得られるに至った。
非破壊でエナメル質中のHAp結晶配向性の観察と定量を行うためには、初期むし歯の形成する領域200 µm幅の領域中の量と質の変化を捉えることが必要となる。それには十分細いビームを表層から深層に向かって当てていき、それぞれの深さのHAp結晶からの回折を観察するという方法が望ましいのは明白であったが、BL40XUの高い平行性を持った高フラックスビームがそれを可能にした。ビームを集光せずにピンホール通過によって直径6 µmにまで細くすることで、表層下脱灰が起こるエナメル表面から深さ200 µmまでを走査するように回折測定ができるようになった(図5a)。さらに、本実験で用いたビームは、非常に直線性の高いビームのため、広角X線回折(WAXRD)と小角X線散乱(SAXS)の両方を測定することが可能である。サンプルにはTMRで用いた厚さ150 µmの歯片をそのまま用いることができた。したがって、TMRとX線回折を行った後もサンプルは非破壊のまま残り、さらなる実験に利用することもできる。最近ではBL40XUの測定はビーム照射位置の移動と測定は自動となっており、サンプル10歯片をセットすると1500枚前後の回折データを3時間程度で得ることができるようになっている。
まずWAXRDについて説明する。エナメル質のHApのc軸はエナメル質表層から歯の内側へ向かう方向へそろっているため、サンプルのセット時にc軸の向きをビームに対してほぼ垂直に置くことができるが、サンプルによっていくらか傾いている。そのため、結晶量の定量のためにc軸の傾きで大きく強度が変化しない(100)面からの反射を用いることとした(図5b)。(100)由来の反射強度を積算し、積算強度をエナメル表層からの深さに対してプロットしていくことにより、TMRのミネラルプロファイルに対応するような結晶量のプロファイルが得られた(図5c)。再石灰化による結晶量の変化は、ミネラルの変化と同様に表層下で回復する様子が観察された。また、同一歯片の健全部と再石灰化部の回折像を比較すると、HApの配向方向がほとんど一致していたこと、また両者で一致しない反射が見られなかったことから、再石灰化で生じた結晶は、元の健全な歯と同じ方向に規則正しく配向していることが確認された。
一方、SAXSではWAXRDの場合と逆に、健全部ではほとんど強度が得られないのに対し、脱灰部と再石灰化部で表層下に強度のピークが現れた(図5d)。これは、HApの結晶小柱が抜けたときに生じる隙間が結晶と同様に一定方向に配向するため、隙間の壁からの散乱がSAXSとして観察されると考えられている。SAXSの結果から、脱灰時にHAp結晶がナノメートル単位のレベルで溶出すること、また再石灰化時には隙間がふさがっていくことが検証された。
以上の結果から、脱灰時にはHAp結晶がある単位ごとに表層下から溶出し、再石灰化時にはそれが隙間を埋めるように回復していくことが明らかとなった。なお、隙間を埋める際に、新しい結晶が生じるのか、元々あった結晶が伸びて埋めるのか、それとも横方向に「太る」のかは、エナメル質のHApの配向性が不完全であるため厳密な解析ができず、わかっていない。ただし、in vitroのHAp結晶成長についてのTEM観察では、その両方があり得ることが知られている。
この方法を用いることで、in vitroおよび口腔内での再石灰化においてリン酸化オリゴ糖カルシウムやリン酸化オリゴ糖カルシウムを含むガムによって再石灰化と同様に再結晶化が促進されることを確認している[6][6] 田中美由紀、北迫勇一、二階堂徹、半場秀典、池田正臣他:日本歯科保存学雑誌 52 (2009) 534-542.。

図5 エナメル質のX線解析
(a)サンプルへのX線照射の模式図。(b)エナメル質由来の回折像。黄色の三角形は(100)の反射を表す。(c)WAXRDによる結晶プロファイル(左)とTMRによるミネラルプロファイル(右)の比較。(d)深さに対するSAXA強度のプロット。
7.おわりに
江崎グリコの企業理念は「おいしさと健康」を提供することにある。おいしさは実際に食べて体感できるが、食べ物が健康にどのように関与するかを伝えるのははるかに難しい。われわれは、科学的な知見に基づいた確かな技術を活用することで、少しでも健康の増進につながる商品作りと情報提供ができると考え、基礎研究を行ってきた。
今回の結果をもとに、江崎グリコはリン酸化オリゴ糖カルシウムを含むガム「フラットスタイルPOs-Ca」の特定保健用食品(トクホ)の許可を2010年9月に得た(表)。トクホの許可表示は、そこに記載されている有効性と作用機序が科学的に検証されたことを保証する。以前にもリン酸化オリゴ糖カルシウムを含むガムとして「ポスカム」を販売していたが、今回のPOs-Caの許可表示では再石灰化とともに再結晶化を促進することが明記されることとなった。このような歯に対する効果を的確に表す情報は消費者のベネフィットにつながると確信している。新しく得たトクホの許可表示を基にした製品は、ポスカム誕生以来8年目になる2011年春に販売開始予定である。
表1 SPring-8の成果を活用した特定保健用食品の許可表示の変化
| 商品名 | 許可表示内容 | 表示許可日 |
| ポスカム | 本品はリン酸化オリゴ糖カルシウム(POs-Ca)を配合しているので、口内を歯が再石灰化しやすい環境に整え、歯を丈夫で健康にします。 | H15.1.21 |
| ポスカ | 初期むし歯(初期う蝕)は脱灰からはじまります。本品は、リン酸化オリゴ糖カルシウムを配合しているので、カルシウムイオンが歯に浸透して脱灰部位が再石灰化と再結晶化しやすい口内環境に整え、丈夫で健康な歯を保ちます。 | H22.9.30 |
産業界がSPring-8を利用するのは「敷居が高い」と思われることも多いようである。しかし、多くのビームタイムとSPring-8スタッフの方々の多大なるご尽力を賜りながら紡ぎだした本研究の構造解析データは、消費者である一般の方、科学技術とわれわれ企業との間をつなぐ、商品というもうひとつの輪に昇華させることができた。われわれのケースは幸運に恵まれた例外的なものであるかもしれないが、SPring-8の測定環境の充実とスタッフの手厚いサポート体制により、産業分野からも今後さらに多くの成果が得られるのは間違いないだろう。
今後も、われわれはSPring-8をはじめとする最先端技術を用いて、確かな知見に基づいて人々の健康に貢献できる商品づくりを目指していく所存である。
謝辞
本研究に関する実験はSPring-8利用課題2007A2095、2007A0102、2007A1945、2008B1995、2009A1851、2009A1885、2010A1278、2010B1829で行われたものです。BL40XUの八木直人博士、太田昇博士、松尾龍人博士に厚く御礼申し上げます。
参考文献
[1] M. R. T. Filgueiras, D. Mkhonto and N. H. De Leeuw: J. Cryst. Growth 294 (2006) 60-68.
[2] S. Saber-Samandari and K. A. Gross: Acta Biomater. 5 (2009) 2206-2212.
[3] H. Kamasaka, M. Uchida, K. Kusaka, K. Yoshikawa, K. Yamamoto et al.: Biosci. Biotechnol. Biochem. 59 (1995) 1412-1416.
[4] H. Kamasaka, D. Inaba, K. Minami, S. Imai and M. Yonemitsu: J. Dent. Hlth. 52 (2002) 105-111.
[5] H. Kamasaka, S. Imai, T. Nishimura, T. Kuriki and T. Nishizawa: J. Dent. Hlth. 52 (2002) 66-71.
[6] 田中美由紀、北迫勇一、二階堂徹、半場秀典、池田正臣他:日本歯科保存学雑誌 52 (2009) 534-542.
[7] N. Yagi, N. Ohta, T. Matsuo, T. Tanaka, Y. Terada et al.: J. Synchrotron Rad. 16 (2009) 398-404.
[8] T. Tanaka, N. Yagi, T. Ohta, Y. Matsuo, Y. Terada et al.: Caries Res. 44 (2010) 253-259.
小林 隆嗣 KOBAYASHI Takatsugu
江崎グリコ(株) 健康科学研究所
〒555-8502 大阪市西淀川区歌島4-6-5
TEL:06-6477-8390 FAX:06-6477-8362
e-mail:kobayashi-takatsugu@glico.co.jp
田中 智子 TANAKA Tomoko
江崎グリコ(株) 健康科学研究所
〒555-8502 大阪市西淀川区歌島4-6-5
TEL:06-6477-8390 FAX:06-6477-8362
e-mail:tanaka-tomoko-2@glico.co.jp
滝井 寛 TAKII Hiroshi
江崎グリコ(株) 健康科学研究所
〒555-8502 大阪市西淀川区歌島4-6-5
TEL:06-6477-8390 FAX:06-6477-8362
e-mail:takii-hiroshi@glico.co.jp
釜阪 寛 KAMASAKA Hiroshi
江崎グリコ(株) 健康科学研究所
〒555-8502 大阪市西淀川区歌島4-6-5
TEL:06-6477-8390 FAX:06-6477-8362
e-mail:kamasaka-hiroshi@glico.co.jp








