Volume 26, No.2 Pages 133 - 137
1. 最近の研究から/FROM LATEST RESEARCH
長期利用課題報告4
中空構造をもつ巨大自己集合錯体分子群の単結晶X線構造解析と機能創出
Synchrotron Studies on Self-Assembled Huge Metal Complexes Toward Their Applications
東京大学 大学院工学系研究科 School of Engineering, The University of Tokyo
- Abstract
- 我々のグループでは、金属イオン(M)と有機分子(L)の間における配位結合の形成に基づく、配位駆動自己集合によるナノ空間のデザインと機能創出を追求してきた。1990年、留め金状の金属錯体と棒状有機配位子の混合により、正方形型の大環状分子がひとりでに組み上がることを初めて報告して以来、様々な構造や性質の内部空間をもったケージ分子を開拓している。とりわけMnL2n型球状錯体の登場以後、その構成分子数の多さや内部空隙の巨大さから構造決定の要である単結晶X線構造解析に困難が伴い、放射光X線の利用が研究遂行に不可欠な要素となっている。近年も、自然界のタンパク質に匹敵するほどのサイズをもつ種々の中空錯体群の構造解析を構造生物学ビームラインの利用を通して進めており、機能創出に向けた取り組みと併せて報告する。
1. はじめに
複数の分子が自律的に集まることで秩序をもった構造を形成する現象を「自己集合」と呼ぶ。自然界においては、コラーゲンの三重らせん形成による堅牢な繊維状構造の実現から、100以上のタンパク質からなる数十ナノメートル径の球状ウイルス殻構造に至るまで、可逆的な分子間相互作用の集積により多様な自己集合システムが機能している。一方、我々のグループでは、人工系における金属イオンと有機分子の配位結合形成を駆動力とした自己集合をベースとした、様々な一義構造を有するナノサイズ中空分子の構築とその機能発現について研究してきた。とりわけ、金属イオン(M)まわりの配位様式と有機配位子(L)の構造が示す幾何学的性質に着目することで、自己集合構造の合理的なデザインが可能となることを示してきた。
その最たる例として、MnL2n型球状錯体の構築を図1に示す。平面4配位構造をとるPd(II)イオンと折れ曲がった構造の二座配位子を溶液中において混合することで、配位結合形成に駆動された、一義的な多面体構造をもつ中空錯体の形成が観測された。
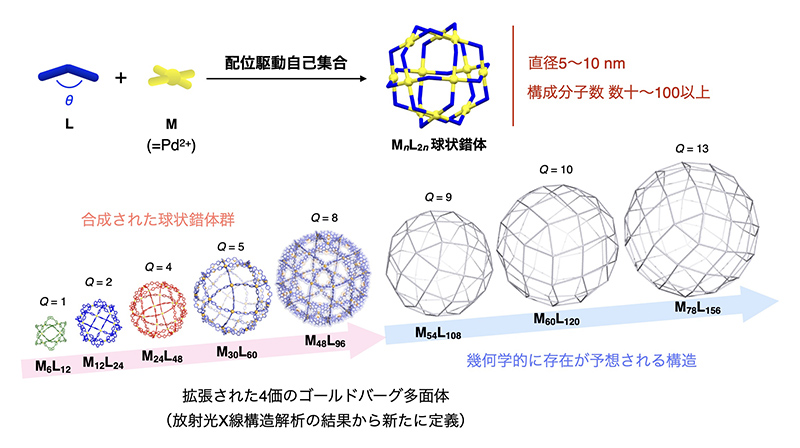
図1 配位駆動自己集合による巨大中空錯体の構築
当初得られたM12L24錯体は36個もの構成分子からなる直径5 nm近い立方八面体構造を示し、この時点で従来知られていた人工系自己集合の概念を飛び越えるものであった。しかしさらに、二座配位子の折れ曲がり角度θや配位子の構造柔軟性を調節することで、アルキメデスの立体(半正多面体)を考えることで予想される、より多くの構成分子からなる錯体群(n = 24, 30)も実際に合成された[1,2][1] K. Harris, D. Fujita and M. Fujita: Chem. Commun. 49 (2013) 6703-6712.
[2] D. Fujita, Y. Ueda, S. Sato, H. Yokoyama, N. Mizuno, T. Kumasaka and M. Fujita: Chem 1 (2016) 91-101.。さらには、幾何学的な制約から存在し得る構造があと1つ(n = 60)で完結するというところで、これまで知られていないタイプの多面体構造をもつM30L60およびM48L96錯体の構築が見出された[3][3] D. Fujita, Y. Ueda, S. Sato, N. Mizuno, T. Kumasaka and M. Fujita: Nature 540 (2016) 563-566.。これらの構造は拡張された4価ゴールドバーグ多面体(無限のバリエーションが予言される)として新たに定義され、合成化学を超えた成果への波及をもたらした。こうして開拓されてきた中空錯体はまた、従来のホスト分子とは異次元の巨大な内部空間の利用により、ナノ粒子の鋳型形成やユビキチンの包接などへ応用されている[1][1] K. Harris, D. Fujita and M. Fujita: Chem. Commun. 49 (2013) 6703-6712.。
2. 配位自己集合における未踏領域への挑戦
巨大中空錯体の構造解析においては、SPring-8における放射光を用いた単結晶X線構造解析が決定的な役割を果たしている。従来の分子構造解析では、核磁気共鳴(NMR)による溶液解析や各種質量(MS)分析も広く用いられてきた。しかしMnL2n型中空錯体の解析過程においてはその巨大構造ゆえ、NMRにおけるT2緩和時間の短さに起因したシグナルの激しいブロードニングや、MSピークの検出困難といった障壁に直面することとなった。X線構造解析についても、ラボ機の性能向上が近年目覚ましいとはいえ、我々のMnL2n中空錯体では最小の部類に入るM12L24錯体の骨格をおぼろげながら観測できる程度の回折データを得るのがやっとの状況である。数ナノメートルに及ぶ巨大な球状構造を有する錯体が配列した単結晶における格別の溶媒含有率(max. 80−90%)が、結晶の堅牢性や回折強度の著しい低下を招いていると考えられる。これに対し威力を発揮したのが、放射光X線によるタンパク質結晶構造解析のノウハウである。タンパク質もまた、直径が数~数十ナノメートルに達し、かつ結晶溶媒を豊富に含む単結晶を生成しやすいことから、良好な回折データ取得のための測定手法が種々開発されている。そこで我々のグループでは構造生物学ビームラインの協力を仰ぎつつ、タンパク質結晶に対して培われてきた知見を人工系における巨大自己集合構造の解析へ持ち込むことで、構造決定を達成してきた。
最近では、折れ曲がり角度を極限まで大きくした二座配位子とPd(II)イオンとの自己集合により、原子間力顕微鏡(AFM)による観察において直径10 nmを超えるようなナノ構造体の形成が観測されている(図2)。微小な単結晶の作製には成功しているものの、やはり回折強度の脆弱さに直面しており、複数の微結晶から得られる回折データを統合的に扱う測定手法や解析法[4][4] M. Yamamoto, T. Kumasaka et al.: IUCrJ 4 (2017) 529-539.などを試みている。また、同じくタンパク質の構造解析に威力を発揮しているクライオ電子顕微鏡による観察および粒子解析技術との組み合わせにより、構造解析の統合的な活用にも着手している。さらに巨大な球状錯体の構築は、タンパク質の包接[5][5] D. Fujita, K. Suzuki, S. Sato et al.: Nat. Commun. 3 (2012) 1093.とその構造・機能制御といった従来のケージ分子では考えられなかった応用への観点からも必要とされており、さらなる開発研究を進めている。
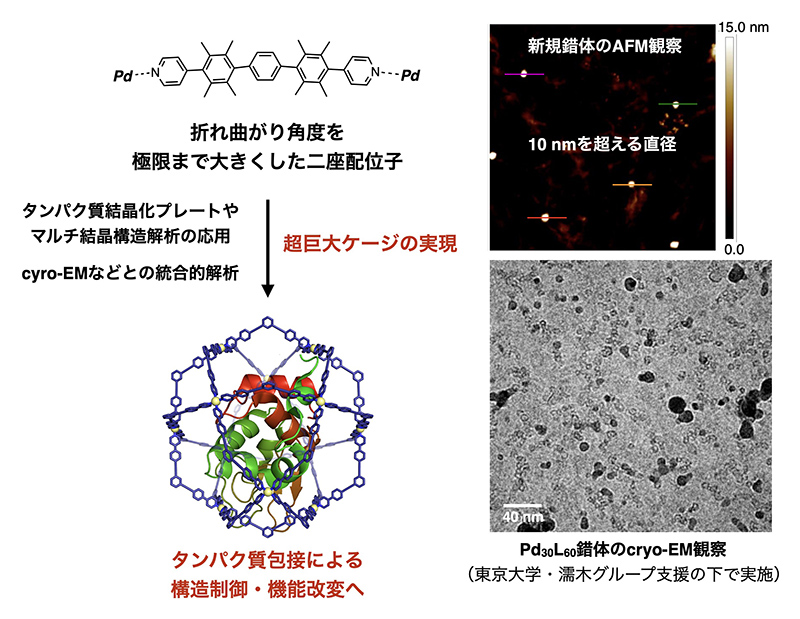
図2 10 nmを超える超巨大ケージの構築と応用を目指した取り組み
上述のように、我々のグループが対象とする自己集合性「分子」は、従来の分子構造解析の技術限界を超えた領域へと突入している。キャラクタリゼーションの観点から険しい道のりの続く研究ではあるが、合成化学の立場から分析技術の飛躍に向けた刺激を与えるという点からも、有意義な試みとして期待される。
一連の取り組みにおいて、放射光X線を用いた結晶構造解析は極めて重要な役割を果たしている。以下、長期利用課題におけるビームライン利用(BL38B1、BL26B1、BL41XU)を通して実現した2つの新たな自己集合システムの創出について紹介する。
3. 配位駆動の進化:弱い配位と強い配位の協働による複雑ナノ構造の構築法開拓
配位自己集合によるナノ構造の構築は近年多様な拡がりをみせている一方で、用いられる配位ドナーは含窒素複素環(例:ピリジン環)やカルボキシレートといった、比較的結合力の強く高い方向規定性をもつものにほぼ限られてきた。これに対し我々は最近、各種有機金属反応において良く知られた配位様式である、金属−不飽和結合間のπ配位を利用した新たな自己集合の開拓を進めている[6,7][6] Y. Domoto, M. Abe, T. Kikuchi and M. Fujita: Angew. Chem. Int. Ed. 59 (2020) 3450-3454.
[7] Y. Domoto, M. Abe, K. Yamamoto, T. Kikuchi and M. Fujita: Chem. Sci. 11 (2020) 10457-10460.。
プロペラ状構造とアセチレンスペーサーをもつ三座配位子(L、図3)とCu(I)イオンの錯形成を検討する過程で、溶液中における1H NMRおよび分子拡散係数の違いによるスペクトルの分離(DOSY)を用いた追跡から、配位子が2つの異なる化学的環境下におかれた直径2.5 nm程度の単一構造形成が観測された。最終的に単結晶X線構造解析により、3つの金属イオンを介した金属−アセチレン相互作用と金属−ピリジル配位の協働により2つの配位子が二重プロペラ型に重なった構造(Cu3L2)が安定化され、これが形式的に2量化することで、(Cu3L2)2組成のケージ錯体を形成することが明らかとなった。
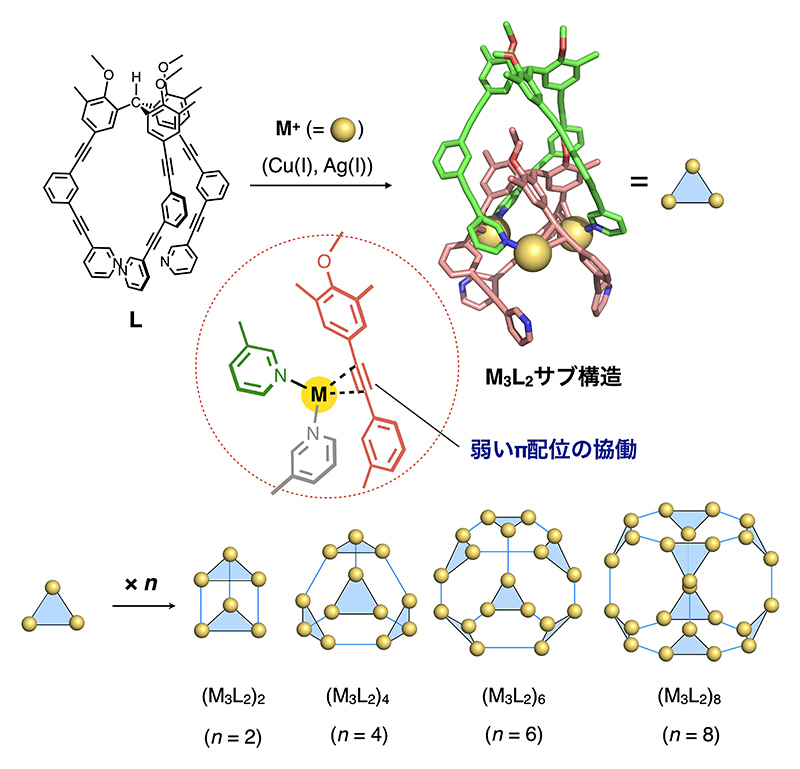
図3 強い配位と弱い配位の協働による多面体錯体群の自己集合
この知見に基づき、金属のイオン半径や溶媒極性、さらに内部に包接する対アニオンのテンプレート効果など錯形成条件を種々探索することで、M3L2(M = Cu+, Ag+)サブ構造が4,6,8個、階層的に集合した中空錯体群をそれぞれつくり分けることに成功した。一連の構造は分子量が8,600~25,000、球体近似した直径が3~5 nmに達し、放射光X線による回折測定を経て初めて結晶構造解析が可能となった。特にX線照射による損傷を受けやすい単結晶についてはヘリカルスキャンによる回折データ取得を採用しており、また、(Ag3L2)8立方体錯体の構造解析においては、複数の結晶から得たデータを統合することで所望の分解能での構造解析を達成した。また一連の多面体構造を詳細に解析した結果、2つに重なった三ツ又モチーフ(=M3L2サブ構造)が多面体の各辺上でらせん状にねじれて接続することで、高度に絡まったキラルな3次元構造の構築が統一的に理解できることがわかった(図4、論文投稿中)。これらの中空錯体は、協働する金属−アセチレン配位の結合力の‘弱さ’と緩やかな方向規定性に起因した高い構造柔軟性を示し、この特性に基づく新たな構造変換過程(多面体への金属挿入)も見出されている。従来、強い配位一辺倒であった配位自己集合によるナノ構造構築に、弱い配位との協働という新たな戦略を導入することで、ナノ空間の構造柔軟性や動的特性を制御できるのみならず、高度に複雑な3次元構造のデザインを可能とする手法の開拓を進めている。
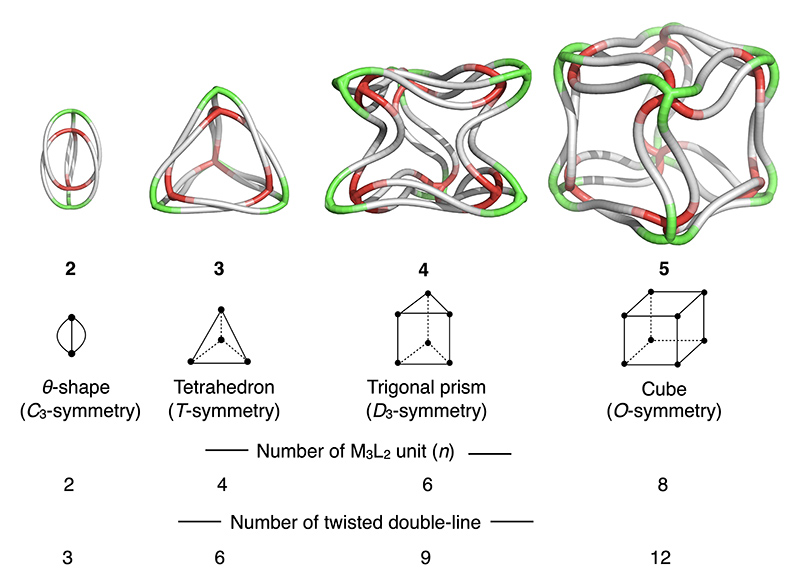
図4 自己集合条件によりつくり分け可能な多面体構造群における高度な絡まり
4. 自然界を凌駕する自己集合へ:ペプチドのフォールディング集合による「人工タンパク質」創出の試み
近年我々のグループでは、金属イオンと数残基のペプチド配位子の自己集合により、ペプチド鎖を特定の配座へとフォールディングさせる過程と、これらの3次元的配置を精密制御する過程を協奏的に行う戦略(フォールディング集合)[8][8] T. Sawada and M. Fujita: Chem 6 (2020) 1861-1876.を提唱している(図5)。
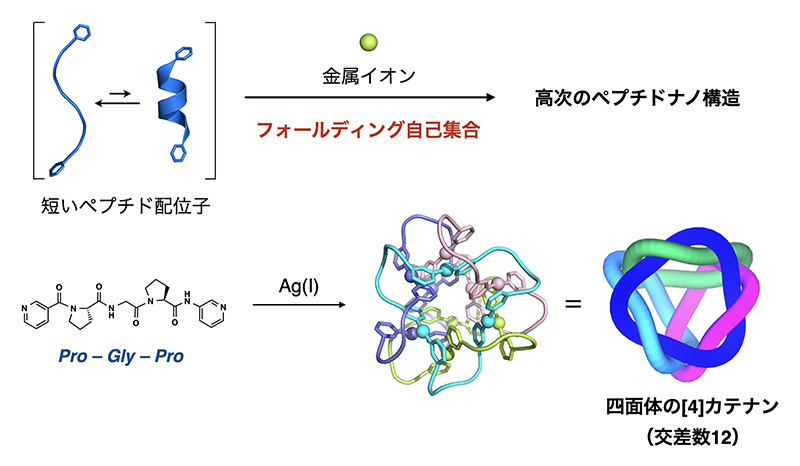
図5 フォールデング集合の提唱
例えば、プロリン−グリシン−プロリン(PGP)の3残基ペプチド配列とAg(I)イオンの錯形成により、ペプチド鎖がΩループ状の配座をとりつつAg(I)イオンと自己集合することで、複雑な絡まり構造をもつ[4][4] M. Yamamoto, T. Kumasaka et al.: IUCrJ 4 (2017) 529-539.カテナン構造(交差数12)が得られている。溶液中において金属イオンと配位子を混合するだけで、単独では複数のコンフォメーションをとり得るペプチド鎖を単一の配座に収束させ、複雑な秩序構造を実現するプロセスは、自然界におけるタンパク質の自己集合を彷彿とさせる。この知見を発展させることで、さらに高次の(交差数24)[6][6] Y. Domoto, M. Abe, T. Kikuchi and M. Fujita: Angew. Chem. Int. Ed. 59 (2020) 3450-3454.カテナンが構築されている[9][9] M. Yamagami, T. Sawada and M. Fujita: J. Am. Chem. Soc. 140 (2018) 8644-8647.。この錯体は外径が3.7 nmの球状であり、内部に3000 Å3もの空孔をもつウイルスキャプシドに類似した構造を有する(図6)。

図6 (a) キャプシド構造をもつ高次カテナン、および、(b) 人工β-バレル構造の構築。
また、フォールディング集合の概念を適用することで、タンパク質の三次構造の1つであるβ-バレル構造を人工的に構築することにも初めて成功している[10][10] T. Sawada, Y. Inomata, K. Shimokawa and M. Fujita: Nat. Commun. 10 (2019) 5687.。β-バレルはβ-ストランドを束ねてループ状に連結した構造をもつが、溶解性の乏しさと形状制御の点から人工合成は困難とされてきた。これに対して、1つの配位子内にβ-ストランドを形成するペプチドと、ループ状構造をとる先述のP-G-Pペプチドを併せもつ配位子を設計することで一連の課題をクリアし、空孔をもつ人工β-バレルの構築と構造解析を達成した。
フォールディング自己集合により、タンパク質の自己集合にみられる集合様式やモチーフを人工系に翻訳することで、タンパク質の構造特性や酵素機能をハイブリッド的に取り入れた人工タンパク質ともいうべき新たなナノマテリアルの構築がさらに期待される。
5. まとめと今後の展望
本稿にて紹介した最近得られてきた巨大な自己集合構造は、微小な単結晶しか得られない場合も多く、また単位格子が100 Å前後の軸長を示すこともしばしばであるのに加え、錯体の中空構造に由来する結晶溶媒含有率が大きくなるのが必然となっている。研究の進展とともに、構造解析の(潜在的な)難易度はますます上がっていくとみられるが、例えば現在進行中の課題では東京大学社会連携講座・佐藤宗太博士らの参画を得て、タンパク質結晶化プレートを用いたin-situ回折測定やマルチ結晶構造解析といった最新の測定技術を我々の人工系試料へと導入する試みも開始している。今後も、分子デザインと構造解析技術における相乗的な進展を図ることで、従来考えも及ばなかったスケールの自己集合構造体を構築し、それらがもたらす内部空間における新たな機能の創造に挑戦していきたい。
最後にこの場を借りて、本長期利用課題(2018A0154~2019A0154、2018B0157~2019B0157、2019A0167~2019B0167)において測定実験および解析のあらゆる場面でご助力を賜ったSPring-8構造生物学ビームライン関係者の方々に対し、共同研究者を代表して深く感謝の意を表する。
参考文献
[1] K. Harris, D. Fujita and M. Fujita: Chem. Commun. 49 (2013) 6703-6712.
[2] D. Fujita, Y. Ueda, S. Sato, H. Yokoyama, N. Mizuno, T. Kumasaka and M. Fujita: Chem 1 (2016) 91-101.
[3] D. Fujita, Y. Ueda, S. Sato, N. Mizuno, T. Kumasaka and M. Fujita: Nature 540 (2016) 563-566.
[4] M. Yamamoto, T. Kumasaka et al.: IUCrJ 4 (2017) 529-539.
[5] D. Fujita, K. Suzuki, S. Sato et al.: Nat. Commun. 3 (2012) 1093.
[6] Y. Domoto, M. Abe, T. Kikuchi and M. Fujita: Angew. Chem. Int. Ed. 59 (2020) 3450-3454.
[7] Y. Domoto, M. Abe, K. Yamamoto, T. Kikuchi and M. Fujita: Chem. Sci. 11 (2020) 10457-10460.
[8] T. Sawada and M. Fujita: Chem 6 (2020) 1861-1876.
[9] M. Yamagami, T. Sawada and M. Fujita: J. Am. Chem. Soc. 140 (2018) 8644-8647.
[10] T. Sawada, Y. Inomata, K. Shimokawa and M. Fujita: Nat. Commun. 10 (2019) 5687.
東京大学 大学院工学系研究科
〒113-8656 東京都文京区本郷7-3-1
TEL : 03-5841-1265
e-mail : domoto@appchem.t.u-tokyo.ac.jp
東京大学 大学院工学系研究科
(JSTさきがけ研究者 兼任)
〒113-8656 東京都文京区本郷7-3-1
TEL : 03-5841-0365
e-mail : tsawada@appchem.t.u-tokyo.ac.jp
東京大学 大学院工学系研究科
(分子科学研究所 特別研究部門 兼任)
〒113-8656 東京都文京区本郷7-3-1
TEL : 03-5841-7256
e-mail : mfujita@appchem.t.u-tokyo.ac.jp








