Volume6 No.1
SPring-8 Section A: Scientific Research Report
ハイドロキシアパタイトをベースとした抗菌性材料の開発に向けたAgおよびCuの局所構造評価
Local Structural Evaluation of Ag and Cu for the Development of Antibacterial Materials Based on Hydroxyapatite
a東北大学 金属材料研究所, b大阪府立大学
aInstitute for Materials Research, Tohoku University, bOsaka Prefecture University
- Abstract
-
高い抗菌性を有する高組織代替材料の開発を目指し、ハイドロキシアパタイト(HAp)合成時にAgおよびCuを添加した試料に対して、Ca、AgおよびCu K吸収端XAFS測定を行った。その結果、Agは添加した量の大部分が金属Agとして存在しており、HAp構造中に固溶し難いことがわかった。また、いずれの元素添加試料においてもリン酸化合物と類似した局所構造を有しており、HAp構造中への固溶の可能性が示唆された。
キーワード: ハイドロキシアパタイト、抗菌、XAFS
背景と研究目的:
チタンおよびその合金は、歯科および整形外科の分野において人工関節や脊髄固定具などの整形外科インプラント用または歯科用インプラントに広く使われている。この整形外科的手術においてよくある合併症の一つが細菌感染であり、10% 程度とされているインプラント治療における失敗例の大部分を占めている[1]。そのため、術中・術後の感染を予防できる新しいインプラントの開発が強く望まれているものの、現時点で抗菌作用を有するインプラントは市場に出ることはもちろんのこと、研究レベルにおいても使用する生体材料に抗菌性を付与する技術はまだ確立されていない。もし、既製品の生体活性を損なわずに、抗菌性を付与する技術があれば、超高齢化の社会の我が国において、インプラント治療はより安心・安全な治療法となり、長い人生における高いQOLが保障される。上記の感染を抑えるための手法としては、チタン表面の抗菌化処理、抗菌性イオンを置換固溶したHApのコーティングが挙げられ、有機物系、無機物系などの抗菌性材料がある中で、金属元素による抗菌性の付与に関する研究が多く行われている。金属元素の中には、人体に対して限界量以下では害を及ぼさず、かつ抗菌性を示すものがいくつか存在していることが知られており、中でも、銀、亜鉛、銅は微量でも強い抗菌性を示すことが知られている[2]。金属の抗菌性は金属がイオンとして溶出することが前提となっており、硫黄、窒素、酸素などを持つ電子密度の高い官能基と反応して溶解度の小さい塩や錯体を形成して機能の不活性化をもたらすことで、抗菌性が発現していると考えられている[3]。したがって、インプラント表面の抗菌化処理、抗菌性元素を固溶したHApのコーティングいずれにおいても、抗菌性元素量を制御し、局所構造および結晶性の変化や、それに伴う生体活性、抗菌特性、生体毒性をバランスよく材料に付加することが基本指針となる。しかしながら、特に抗菌性元素を置換させたHApに関する報告例は、銀および銅が固溶しにくい元素であるため極めて少なく、固溶限や固溶位置等、そのほとんどが明らかとなっていない。
X線吸収微細構造(XAFS)測定は高い元素選択性を有し、また、感度が高いためppmオーダーの微量元素の局所構造測定が可能な手法であり[4]、HApに対して難固溶元素である銀および銅の測定に有効な手法である。著者らはこれまでにHAp中へFe[5][6] およびSi[7] を添加し、これら元素のHAp中への固溶限および局所構造を明らかにしてきた。また、AgおよびCuのリン酸塩におけるXAFSの適用としては、分野は異なるが、エレクトロニクス分野においてZhangら[8] およびZhaoら[9] がリン酸銅を正極物質として用いることでLiイオンバッテリーおよびNaイオンバッテリーを作製し、その充放電におけるリン酸銅の局所構造変化をそれぞれ報告している。
このような背景から、本研究ではHApにAgおよびCuを置換固溶させた置換型HApを合成し、XAFS測定により銀および銅近傍の局所構造を解析し、HAp中へのAgおよびCuの固溶状態および固溶限を明らかにすることを目的とした。
実験:
試料作成
出発原料はCa源として硝酸カルシウム(Ca(NO3)2・4H2O)水溶液、P源としてリン酸水素二アンモニウム((NH4)2HPO4)水溶液、Ag源として硝酸銀(AgNO3)水溶液、Cu源として塩化銅(CuCl2)水溶液をそれぞれ用いた。またpH調整用として 1 M のヒドロキシメチルアミノメタン(CH2(OH)3CNH3;Tris)水溶液および 5 M の水酸化ナトリウム(NaOH)水溶液を用いた。仕込み比として Ca/P 比が 1.67 となるように硝酸カルシウム水溶液を 10 ml とリン酸水素二アンモニウム水溶液を 6 ml それぞれ量りとり、硝酸カルシウム水溶液に硝酸銀水溶液あるいは塩化銅水溶液をCaに対してAgおよびCuがそれぞれ 0、0.5、1、2、5、10 mol% となるように加え、1 M のヒドロキシメチルアミノメタンを用いて pH 8 に調整した。リン酸水素二アンモニウム水溶液は 5 M の水酸化ナトリウム水溶液を用いて pH 12 に調整した。各溶液をテフロン容器内で5分間攪拌しながら混合し、オートクレーブ中に密閉した。オートクレーブを 150℃ の恒温炉で 24 h 静置水熱させた。その後、遠心分離で沈殿物と上澄み液を分離させた後、得られた沈殿物を 50℃ の乾燥炉で一晩乾燥させて試料とした。
XAFS測定
得られた試料の局所構造について検討するために、試料の Ca K 端および Ag K 端、Cu K 端についてX線吸収微細構造(X-ray Absorption fine structure:XAFS)を測定した。Ca K 端XAFSスペクトルはSPring-8 BL01B1にて透過法により測定した。分光器にはSi(111)(d = 3.13551 Å)を用いた。測定用粉末はメノウ乳鉢、乳棒を用いて窒化ホウ素(BN)とアセトン中にて30分程度湿式混合し、ペレット成形後にメンディングテープに挟み測定用試料とした。ペレットを作製する際の試料の重量は試料調整ソフトウエアXAFS_Sampleにより計算し、試料 2.09 mg、BN 34.71 mg、直径 10 mm、厚さ 0.2 mm、BN吸収率 82.6% とした。Ag K 端および Cu K端のXAFSスペクトルはSPring-8 BL01B1にて19素子Ge-SSD検出器を用いた蛍光法により測定した。得られたスペクトルはAthenaを用いて解析を行った。
結果および考察:
表1に測定に供した試料のICPを用いた組成分析結果を示す。Cu添加試料では添加量が 2 mol% 以下の試料では、添加量と含有量が比較的近い値となったが、5 および 10 mol% の試料では添加量に対して含有量が低い値となりその含有量は 3 mol% 程度であった。一方、Ag添加試料では、Ag添加量増加に伴ってAg含有量は増加しているが、添加量に対して含有量は著しく低い値となった。これより添加したAgの大部分は試料中に含まれておらず、HAp構造中に固溶していないことが示唆される。また、X線回折測定より、全ての試料はHApに帰属可能な回折ピークのみが得られており、第二相の存在は確認されなかった。
表1. ICP による組成分析結果
| Sample | Cu (mol%) | Ca/P ratio | Sample | Ag (mol%) | Ca/P ratio | 0.5%Cu | 0.392 | 1.62 | 0.5%Ag | 0.002 | 1.64 | 1.0%Cu | 0.952 | 1.61 | 1.0%Ag | 0.027 | 1.64 | 5.0%Cu | 2.540 | 1.60 | 5.0%Ag | 0.241 | 1.66 |
図1に(a)参照試料および(b)Ag添加およびCu添加HAp粉末のCa K吸収端XANESスペクトルを示す。得られたXANESスペクトルは、Ag添加HAp、Cu添加HApいずれも元素添加量の増加に伴うピークシフトおよびスペクトル形状の変化は見られなかった。また、参照試料のXANESスペクトルとの比較から、いずれも市販品のHAp200と類似したスペクトルが得られており、AgおよびCu添加に伴うCaイオンの局所構造変化は生じていないことが示唆された。
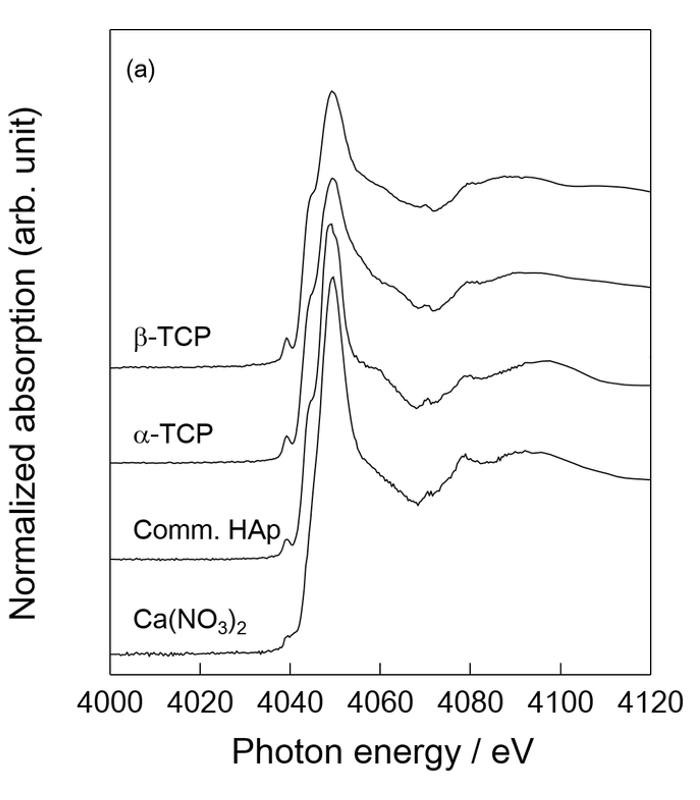
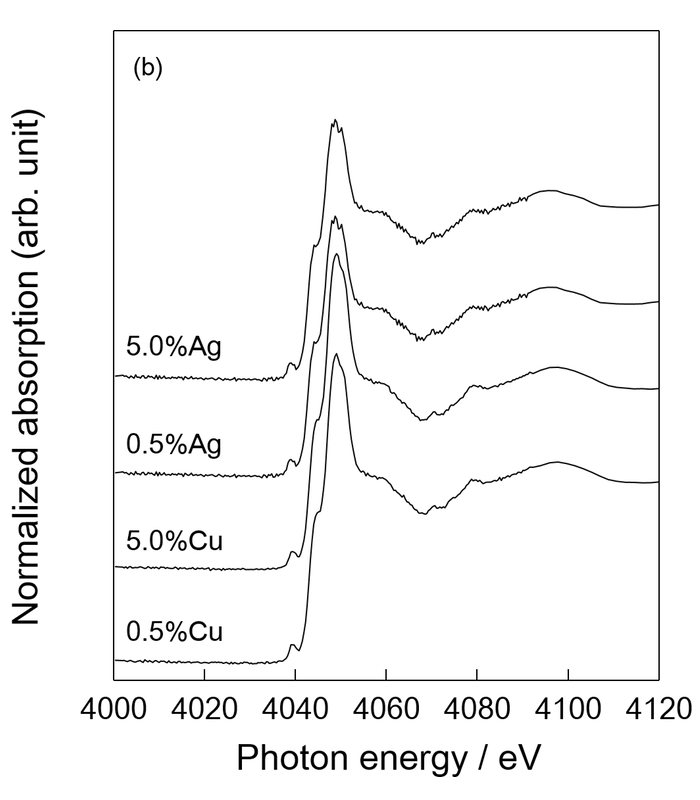
図1. (a) 参照試料および (b) Ag添加およびCu添加HAp粉末の Ca K 吸収端XANESスペクトル
図2に市販のHAp粉末、Ag添加およびCu添加HAp粉末の(a) EXAFSスペクトルおよび(b)フーリエ変換により得られた動径分布をそれぞれ示す。EXAFSスペクトルは k3 の重み付けをし、また、k > 10 ではノイズの影響が大きくなるため、3 < k <10 の範囲での解析を行った。Ag添加およびCu添加HAp粉末いずれも、EXAFSスペクトルの位相および振幅、動径分布より得られる Ca-O および Ca-P の結合距離、配位数等に大きな変化が見られず、XANESの結果同様、今回の解析範囲における元素添加の影響は見られなかった。
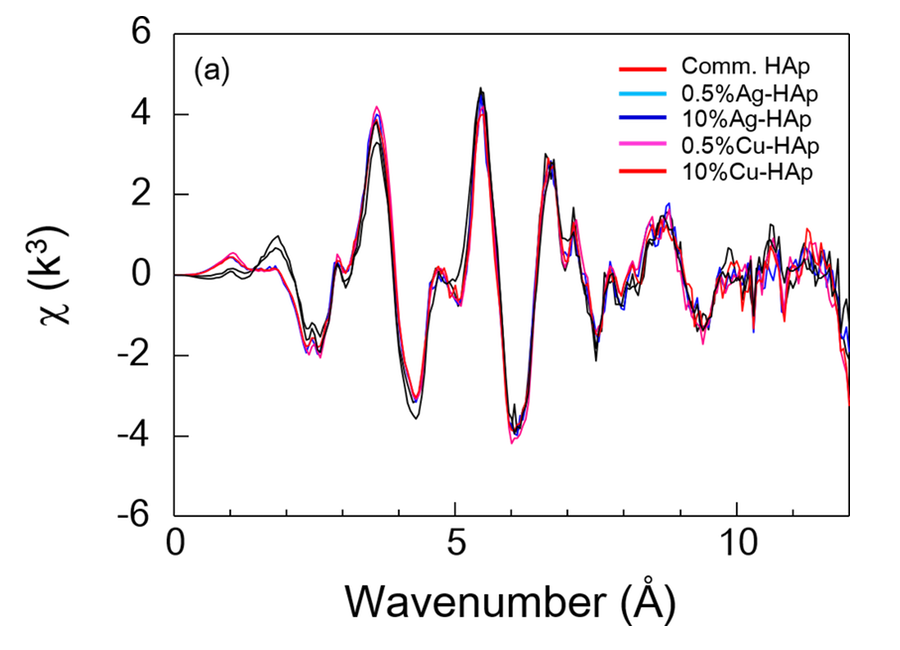
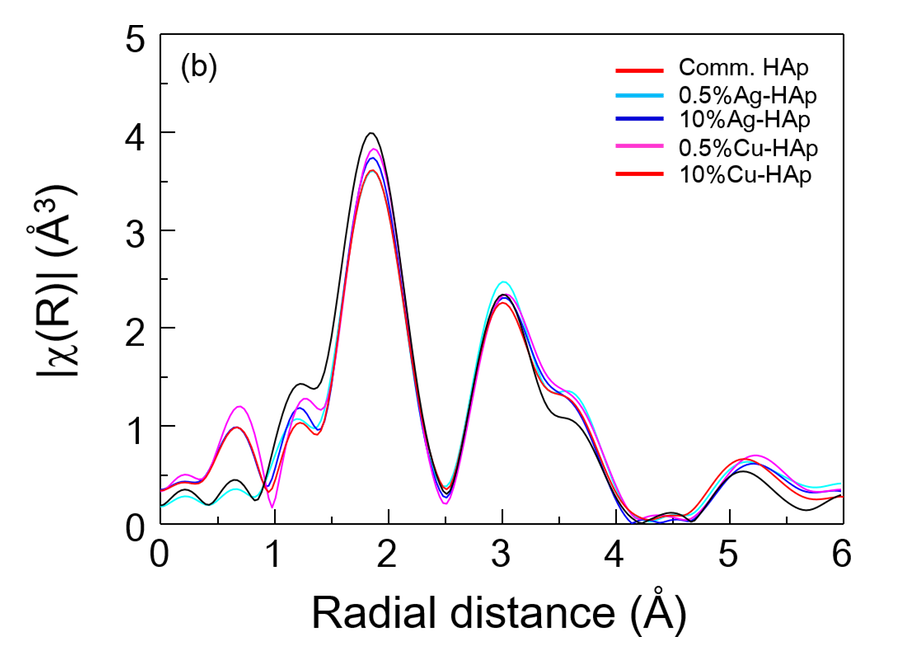
図2. HAp粉末、Ag添加およびCu添加HAp粉末の (a) EXAFSスペクトルおよび (b) フーリエ変換により得られた動径分布
図3に (a)参照試料および(b) Ag添加HAp粉末のAg K吸収端XANESスペクトルを示す。得られたXANESスペクトルは、Agの高添加量において金属Agのスペクトルと類似したスペクトルが得られており、添加したAgは金属Agとして存在していることが明らかとなった。一方、低添加量ではスペクトルのピークトップが低エネルギー側にシフトしており、金属Ag以外の化合物相が存在していることが示唆された。そのため、試料のXANESスペクトルに対し、25450 eV から参照試料を含めた全てのスペクトルの等吸収点である 25546 eV の範囲にて Linear combination fitting を用いて今回測定した参照試料それぞれの存在比率を算出した結果、いずれの添加量においても酸化銀や原料である硝酸銀は存在せず、金属Ag、Ag3PO4および Ag4P2O7 のリン酸銀のスペクトルでフィッティングが可能であり、Ag添加量の増加に伴い金属Agの比率が 30% (0.5%Ag-HAp)から 85% (5%Ag-HAp)へと増加した。
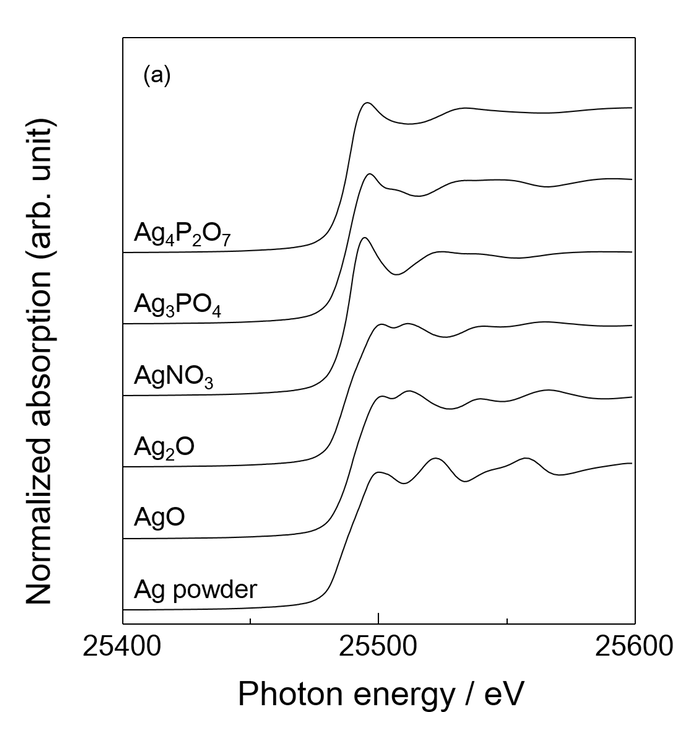
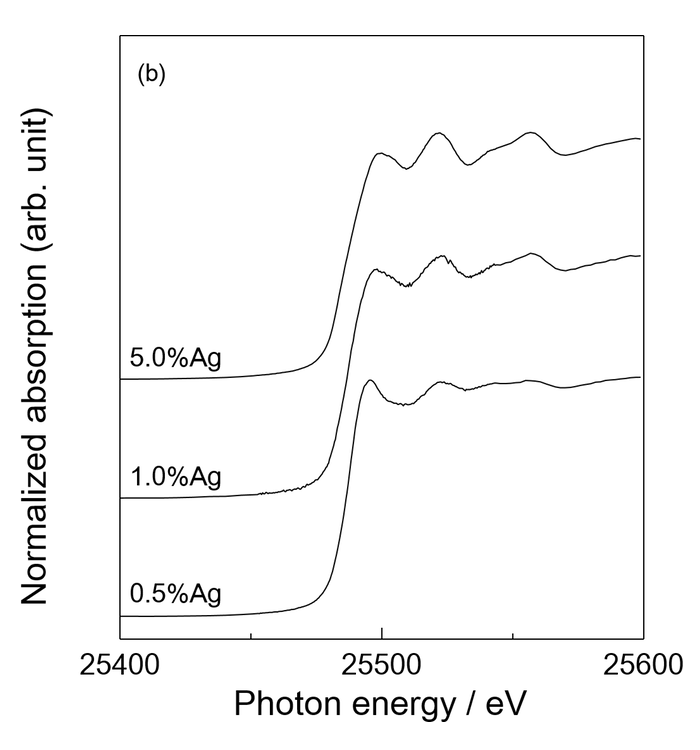
図3. (a) 参照試料および (b) Ag添加HAp粉末の Ag K 吸収端XANESスペクトル
図4に (a)参照試料および(b) Cu添加HAp粉末のCu K吸収端XANESスペクトルを示す。得られたXANESスペクトルは、吸収端のシフトは見られず、添加したCuは2価で存在していることが明らかとなった。また、いずれの添加量においても Cu3(PO4)2 と類似したスペクトルが得られており、Cu原子近傍の局所構造は Cu3(PO4)2 に似た構造を有していることが示唆された。
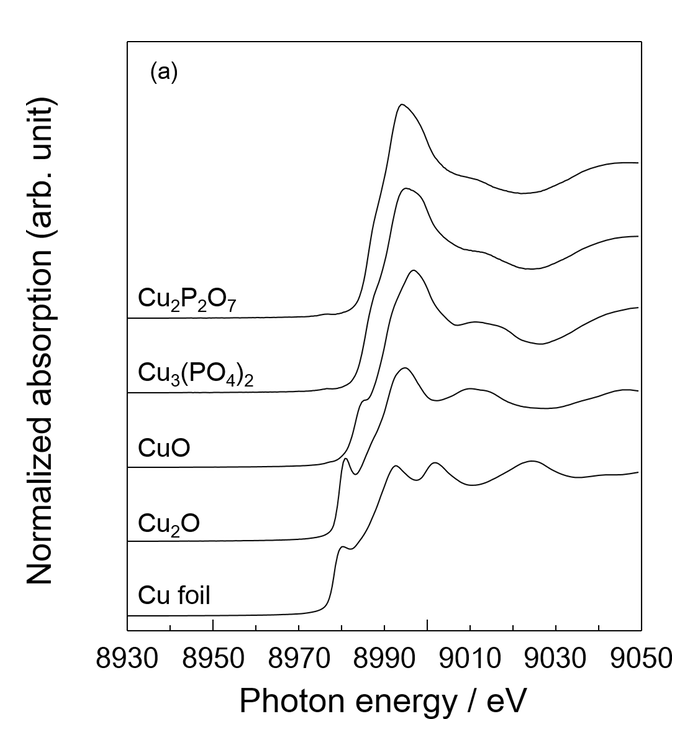
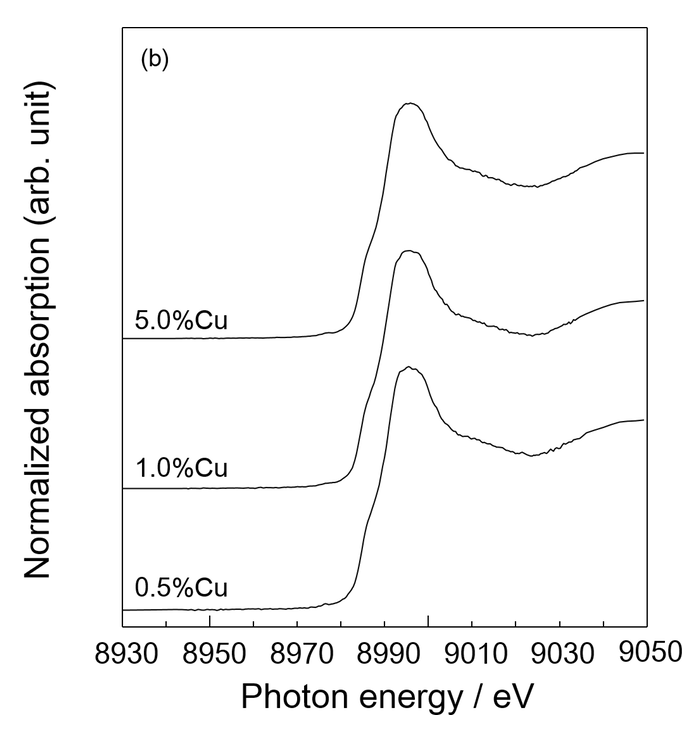
図4. (a) 参照試料および (b) Cu添加HAp粉末の Cu K 吸収端XANESスペクトル
以上の結果から、Ag添加HApでは一部のAgがリン酸銀と、Cu添加HApでは大部分がリン酸銅とそれぞれ似た局所構造を有していることが示唆されており、HAp構造中への固溶している可能性が示された。そのため、今回はXANESスペクトルによる結果の考察を行ったが、今後はEXAFS解析も進め、より詳細な局所構造解析からHAp中のAgおよびCuの化学形態の特定を行う予定である。
参考文献:
[1]C. Hamanishi, J. Jpn. Soc. Biomater., 29 4 240-243 (2011)
[2] 宮野泰征ら, 鉄と鋼 93 57-65 (2007)
[3] L. Sintubin et al., Appl. Microbial. Biotechnol., 91 1 153-162 (2011)
[4] 太田俊明 編, X線吸収分光法 –XAFSとその応用-, アイピーシー, (2002)
[5] M. Sato, and A. Nakahira, J. Ceram. Soc. Jpn., 121 559-562 (2013)
[6] M. Sato, and A. Nakahira, J. Ceram. Soc. Jpn., 121 422-425 (2013)
[7] K. Nakata et al., Mater. Trans., 50 1046-1049 (2009)
[8] G. Zhong et al., Chem. Mater., 27 5736-5744 (2015)
[9] W. G. Zhao et al., Nano Energy, 27 420-429 (2016)
ⒸJASRI
(Received: April 5, 2017; Early edition: November 24, 2017; Accepted: December 18, 2017; Published: January 25, 2018)






