Volume3 No.2
SPring-8 Section A: Scientific Research Report
法科学試料の赤外微量分析
Infrared Microanalysis of Trace Chemicals on Forensic Science
(公財)高輝度光科学研究センター
JASRI
- Abstract
-
微小な法科学試料を、高輝度赤外放射光と通常実験室光源を用い、それぞれ分光スペクトルを測定した。試料サイズと測定領域が小さいほど、赤外放射光の高輝度性が優位に働き、S/N比が高く、吸収度の飽和現象が起こらないスペクトルを得られた。このことから赤外放射光の有用性が確かめられた。
キーワード: 法科学試料、赤外顕微分光、微量分析
背景と研究目的:
通常実験室光源(赤外分光光度計の内部光源、グローバーランプ)による赤外分光に比較して、輝度の高い赤外放射光分光は、微小試料の分析に適している[1-3]。また犯罪遺留物などの分析は、より微量なものを高感度に測定することが求められている[4]。これらのことを背景に、微小な法科学試料の検出、同定に高輝度赤外放射光を用いる事例が増えている。例えば、爆発残渣にわずかに含まれる爆薬成分[5]、日用品や工業製品の多くに含まれる装飾用微小添加物[6]、採取した指紋に残された微量の外来物質[7-9]、自動車塗装皮膜片[10,11]などの分析例があり、いずれの場合も試料が微小なために、高輝度赤外放射光による顕微分光測定が有効である。
本研究では、2011年にBL43IRに導入された赤外顕微分光装置(Bruker社製 赤外分光光度計Vertex70と赤外顕微鏡 Hyperion2000の組み合わせ)を用い、微小な法科学試料(メタミドホス、酢酸タリウム、自動車塗装皮膜片)を用意して、分光スペクトルのクォリティーを保持しながら、どの程度の大きさのものまで検出できるのか、半定量的に比較検討する。
実験:
1.微量のメタミドホス結晶をマイクロピンでフッ化バリウム基板上にのせ、赤外顕微鏡で透過測定を行った。偏光子を光路に挿入し、直線偏光を用いた。試料は大体20-30 μm程度のサイズのものを赤外顕微鏡下で選択した。視野絞りで赤外光を4 μm角の領域に制限して照射した。分光光度計のグローバーランプでも同様に視野絞りを挿入し、得られた赤外スペクトルを比較した。波数分解4 cm-1, 積算128回。
2.食品に混入された微量劇毒物を模して、メタミドホスの50%濃度水溶液を作り、マイクロピンを用いて金属基板上におよそ50-60 μm程度のスポットを作った。視野絞りを2 μm, 5 μm, 8μmに調整して、赤外放射光とグローバーランプの反射測定を行った。
3.食品に混入された微量劇毒物を模して、酢酸タリウム水溶液をスライドガラス上で乾燥させたあとの残留しみを掻き出して得られた微量試料を、マイクロピンでフッ化バリウム基板上にのせ、赤外顕微鏡で透過測定した。試料サイズは数μm以下で、視野絞りは2 μm, 5 μm, 10 μmのものを使った。
4.自動車塗装皮膜片をミクロトームで塗装層が出るように断面カットした。厚さは5 μm。視野絞りを5 μmに調整して、それぞれの塗装層を透過測定した。
結果および考察:
メタミドホス結晶の微小領域を、赤外放射光とグローバーランプでそれぞれ直線偏光測定した透過スペクトルを図1に示す。図1(b), (c)では、グローバーランプのスペクトルに吸収ピークの飽和が見られ、透過光強度が不十分であることがわかる。ここでの吸収ピークの飽和とは、検出器への入射光量が低く、定量下限値付近であるために吸収度の飽和現象が起こることであり、吸収ピークが頭打ちになっているようなピーク形状となって現れ、吸収度と濃度の定量的な関係が崩れている。そのことを確かめるために、さらに厚さのある図1(a)左側結晶のスペクトルを測定すると、図1(d)のように、グローバーランプのスペクトルに、吸収度飽和現象がさらに顕著に見られた。

図1 (a)メタミドホス結晶、図中の両矢印直線は測定偏光方向を示す (b)-(d)それぞれの透過偏光スペクトル(赤)赤外放射光、(青)グローバーランプ
次に結晶ではなく、食品に混入された場合の残留物を模して、濃度の高いメタミドホス水溶液の反射測定を行った。ここでは微小な領域を測定し、二つの光源による違いを見た。図2(b)-(d)に赤外反射スペクトルを示す。

図2 メタミドホス水溶液の赤外反射スペクトル
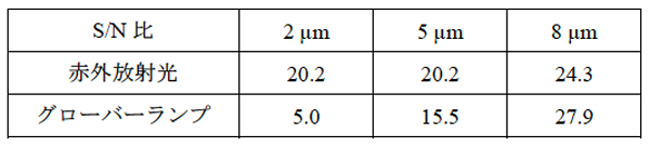
表1に示すように、輝度の優位性を反映して、2 μmと5 μmの視野絞りでは、スペクトルのS/N比における赤外放射光の優位性が明らかである。8 μmの視野絞りでは、優位性は見られない。この試料形態の場合、測定点の面積は狭いが、試料に厚みがあるので、微小なスポット(厚さも薄い)とは状況が違い、試料の濃度と吸収度がある程度確保される。そのためにS/N比の低いグローバーランプでも、吸収ピークの判別は比較的容易である。
表1 光源と視野絞りによるS/N比(RMS: 2300-2500 cm-1)
そこで、実際に微小なスポットで、なおかつ厚さも薄い微量残留劇毒物を模して酢酸タリウム残留しみの透過測定を行った。図3に示すように、この場合には、厚さが薄いため、試料濃度が低いことと同義で、吸収度が低い。そして、赤外放射光の優位性が明らかである。2 μmの視野絞りとグローバーランプでは、図3(b)に示すように、(a)試料ではかろうじて吸収ピークが見て取れるが、図3(e)のように、さらに小さい(d)試料では、ほぼ測定不能である。赤外放射光では、いずれの試料でも有意の吸収ピークが得られている。また、微小試料に対して、それよりも面積の広い視野絞り(10 μm)を挿入して測定した場合、照射光の相当の部分が試料のない基板部分を透過することになるために、吸収度の過小評価現象が起こる。図3(f)に示すように、赤外放射光は輝度が高いことで試料に当たる光強度が高いので、過小評価の状態が解消されるわけではないが、グローバーランプに比べれば吸収度が高く現れる。一方、グローバーランプでは、吸収度の顕著な過小評価が見られる。これらのことから、グローバーランプでの微小試料の測定は難しいことがわかる。

図3 酢酸タリウム残留しみの赤外透過スペクトル
自動車事故での擦過痕を想定して、自動車の塗装皮膜の薄片を透過測定した。塗装皮膜を削り取ったものを、ミクロトームで各塗装層が現れる方向で5 μmの薄片に切削した。図4(a)のように、クリア層、上塗り層、中塗り層、下塗り層、それぞれが数10 μm前後の広さがあるために、図4(b)-(e)の透過スペクトルでは、赤外放射光のグローバーランプに対する優位性は顕著には見られなかった。ただし、今回の塗装皮膜試料は、きれいな状態を保った切削片であり、実際の擦過痕から採取できるものとは異なる。たとえば擦過痕の縁に付着したバリ状の微小残留塗装皮膜片を採取したときに、その同定には赤外放射光の利用が有効であると考えられる。また塗装皮膜内では、顔料や、クロスリンカーとして使われるメラミン樹脂が拡散していて、車種データベースの照合精度を低下させることがわかっている[10]。そのような状況を回避するためには、各層間の境界領域から離れた、他層成分が混在しない純粋な領域を測定する必要がある。そうすると結果的に、測定領域は数μm程度の広さとなり、赤外放射光のグローバーランプに対する優位性が顕著になると考えられる。
メタミドホス、酢酸タリウム微量試料ともに、試料が微小なほど、また視野絞りの小さいほど、赤外放射光がグローバーランプに比べて優位であることが示された。自動車塗装皮膜片は、測定面積、試料厚さ、ともに標準的なために、赤外放射光の優位性は顕著ではなかった。ただし前述のとおり、各塗装層境界を避けると、測定可能面積が格段に小さくなり、赤外放射光で測定することが有用と考えられる。

図4 自動車塗装皮膜各層の赤外透過スペクトル
今後の課題:
今回、微小な劇毒物試料と自動車塗装皮膜片を、ある程度犯罪遺留物を模して試料調製を行い、赤外放射光と分光光度計内部のグローバーランプを用いてスペクトルの比較を行った。今後はより実際の法科学試料に近いもの、たとえば塗装皮膜の部分的な薄片、一本の繊維片、薬物のしみ、また微量劇毒物が食品に混入した混合物試料などの測定を行い、赤外放射光の優位性を検討することが必要である。
参考文献:
[1] T. Moriwaki, Y. Ikemoto, Infrared Physics & Technology 51, 400 (2008).
[2] Lisa M. Miller, Randy J. Smith. Vibrational Spectroscopy 38, 237 (2005).
[3] Erika Levenson, Philippe Lerch and Michael C. Martin, J. Synchrotron Rad. 15, 323 (2008).
[4] Ivan M. Kempson, K. Paul Kirkbride, William M. Skinner, John Coumbaros, Talanta 67, 286 (2005).
[5] A. Banas, K. Banas, M.Bahou, H.O. Moser, L. Wen, P. Yang, Z.J. Li, M. Cholewa, S.K.Lim, Ch.H.Lim, Vibrational Spectroscopy 51, 168 (2009).
[6] Laetitia Vernoud, Hans A. Bechtel, Michael C. Martin, John A. Reffner, Robert D. Blackledge,Forensic Science International 210, 47 (2011).
[7] Ashleigh Grant, T. J. Wilkinson, Derek R. Holman, and Michael C. Martin, Applied Spectroscopy 59,1182 (2005).
[8] A. Banas, K. Banas, M.B.H. Breese, J. Loke, B. Heng Teo and S.K. Lim, Analyst 137, 3459 (2012).
[9] A. Banas, K. Banas, M.B.H. Breese, J. Loke, S.K. Lim, Anal Bioanal Chem 406, 4173 (2014).
[10] Mark Maric, Wilhelm van Bronswijk, Simon W. Lewis, Kari Pitts, Danielle E. Martin, Forensic Science International 228, 165 (2013).
[11] Mark Maric, Wilhelm van Bronswijk, Simon W. Lewis, Kari Pitts, Talanta 118, 156 (2014).
ⒸJASRI
(Received: January 8, 2015; Early edition: March 25, 2015; Accepted: June 29, 2015; Published: July 21, 2015)






