Volume3 No.2
SPring-8 Section A: Scientific Research Report
再生骨の骨質および力学特性に対する全身性微振動および断続的副甲状腺ホルモン(1-34)投与の相乗的作用の解析
Synergetic Effect of Whole-Body Vibration and Intermittent Parathyroid Hormone (1-34) on Regenerated Bone Quality during Defect Healing
大阪大学
Osaka University
- Abstract
-
本研究では、全身性微振動(WBV)と副甲状腺ホルモン(PTH)断続的投与の骨修復促進に対する相乗効果について、卵巣摘除による骨粗鬆症発症マウスおよび健常マウスの脛骨に作製したドリル欠損部を対象に、3次元CTによる形態解析,放射光赤外顕微分光による材料特性解析およびナノインデンテーション試験による力学特性解析による実験的検討を行った。その結果、WBVとPTHの併用は再生骨のネットワーク形態に相乗的に作用することが示唆された。一方、再生骨の材料特性および力学特性への効果は認められなかった。
キーワード: 骨再生,全身性微振動,副甲状腺ホルモン,マイクロCT,放射光赤外顕微分光,ナノインデンテーション試験
背景と研究目的:
骨折はその治癒過程において筋骨格の減少を招き、高齢者においては廃用による要介護や寝たきりのリスクを高める。また、成長期の骨折は一時的な骨成長の減速による成人時の到達ピーク骨量の低下を招き、将来の骨粗鬆症の発症リスクを高める。したがって、骨折治癒の遅延・長期化を回避して促進に転じ、リハビリテーションによる筋骨格機能の早期回復を可能とすることは、骨粗鬆症予防の有効な対策になり得る。
全身性微振動(Whole-Body Vibration,以下、WBV)は、その骨形成効果から、骨修復への効果も期待されており、その有効性は先行研究でも報告されている[1][2]。一方、断続的投与によって骨形成促進に働く副甲状腺ホルモン(Parathyroid Hormone,以下、PTH)は、力学的刺激による骨形成の活性閾値を低下させ、その骨形成促進効果を増強することが指摘されている[3]。これらWBVとPTHの骨形成への作用から、骨折治療における両者の併用は相加・相乗的に有効な効果をもたらすことが期待される。本研究では、マウスの脛骨に作製した欠損部を対象に、WBVと断続的PTH(iPTH)投与の骨修復促進に対する相乗効果について実験的に検討した。
実験:
本研究における実験は、大阪大学大学院基礎工学研究科・動物実験委員会の承認(No.21-1-1)のもとに行った。
試料 9週齢で卵巣を摘出した骨粗鬆症モデル(OVX)と健常のマウス(C57BL,♀,11週齢)の右後肢脛骨の骨幹部に、マイクロドリルで直径0.5 mmの骨欠損を作製した。OVXマウスは通常飼育(OVX-C)群,WBV負荷(OVX-W)群,iPTH投与(OVX-P)群,およびWBV負荷+iPTH投与(OVX-W/P)群の4群に分け、健常マウスは通常飼育した(Sham群)。欠損作製の翌々日より、OVX-W群,OVX-W/P群には、加速度0.3 G,周波数45 Hzの微振動を毎日20分間与え[4]、OVX-C群,OVX-P群,Sham群は、振動ケージに入れるのみとした。加振および振動制御には動電型振動試験装置(SW-2015/ APD-200FCA, Asahi Seisakusyo社製)を用いた。OVX-P群,OVX-W/P群には、PTH(1-34)を30 µg/kg/日で皮下投与した[5]。OVX-W/P群についてはWBV負荷実験開始の30分前に同所へのPTH投与を行った。OVX-C群,OVX-W群,Sham群にはPTHと同量の賦形剤を皮下投与した。
欠損作製20日後に安楽死させ、脛骨を摘出し、欠損部のCT計測を行った。次いで試料をPMMA(ポリメタクリル酸メチル)樹脂に包埋し、鏡面研磨により欠損部横断面を露出させ、皮質骨欠損内の再生骨領域においてフーリエ変換赤外線分光顕微計測(FTIR-MS)およびナノインデンテーション試験を行った。
CT計測 X線CT(SMX-1000/VCT,Shimadzu社製)を用いて骨形態を解析した。CTの撮像条件は、管電圧90 kV,管電流110 mA,ビュー数1200,平均回数5とした。ボクセルサイズは約9 µmであった。得られた三次元データは画像処理ソフト(Image J,National Institutes of Health製)を用いて、Otsu法により閾(しきい)値を決定し、骨部抽出した。欠損部内の円筒形領域を関心領域とし、領域内の再生骨の体積分率と骨梁様の構造指標を算出した。
FTIR-MS FTIR-MS(Bruker Vertex70, Bruker Optics社製)を用いて、再生骨領域のマッピング測定(反射モード,アパチャーサイズ20 µm)により、再生骨材料特性を調べた(図1)。光源にはSPring-8の放射赤外光を利用した。計測条件は、計測波数域700-4000 cm-1,積算回数200回,分解能4 cm-1とした。材料特性パラメータとして、鉱質/有機基質比(リン酸塩帯域[980-1200 cm−1]とI型コラーゲン帯域[1600-1720 cm−1]の面積比),ハイドロキシアパタイト(HA)結晶化度(リン酸塩帯域[980-1200 cm−1]の分離波形のうち、化学量論的HA波形[1030 cm−1ピーク]と非化学量論的HA波形[1020 cm−1ピーク]の面積比)およびコラーゲン架橋度(アミドI帯域[1600-1720 cm−1]の分離波形のうち、ピリジノリン波形[ピーク位置1660 cm−1]とハイドロ-ジヒドロキシリシノノルロイシン波形[ピーク位置1690 cm−1]の面積比)を求めた。
図1.FTIR-MSの計測領域.
ナノインデンテーション試験 FTIR-MSのマッピング領域を対象に、超微小硬度計(DUH-201S,Shimadzu社製)を用いてナノインデンテーション試験を行い、再生骨力学特性を調べた。計測条件(loading-holding-unloading process)は、最大負荷6 mN,負荷速度0.28 N/s,保持時間100 s,除荷速度0.28 N/sとした。力学特性パラメータとして、押し込み弾性率および硬さを求めた。
結果および考察:
CT計測による再生骨形態の計測結果を図2に示す。再生骨の体積分率について、OVX-P群(0.56±0.16), OVX-W/P群(0.56±0.17)はOVX-C群(0.37±0.16),OVX-W群(0.37±0.20)に対して有意に高値を示した。骨梁幅(µm)について、OVX-P群(89±25)は、OVX-C群(68±20)に対して有意に高値を示した。骨辺数密度(/mm3)について、OVX-W/P群(12894±5226)はOVX-C群(8702±4067),OVX-W群(7577±3257)に対して有意に高値を示し、Sham群(9990±1797)を上回る値であった。結合数密度(/mm3)については、群間に有意な差は見られなかった。骨辺数密度においてOVX-W/P群のみがOVX-C群に対して有意な差が見られたことから、WBVとiPTHの併用は再生骨のネットワーク形態に相乗的に作用することが示唆された。一方、iPTH単独では、骨梁幅の有意な増加が見られたにもかかわらず、WBVと併用することで、OVX群との有意な差は確認できなくなった。すなわち、WBVはiPTHの骨梁幅の増加に対する効果を抑制し、相乗的な骨辺数増加は骨体積分率の増加をもたらさなかった。
FTIR-MSおよびインデンテーション試験による再生骨の材料特性および力学特性の計測結果を、それぞれ図3および図4に示す。いずれのパラメータについても群間に有意な差は認められなかった。このことから、少なくとも本モデルにおける回復期間20日では、WBV,iPTH,およびWBVとiPTH併用のいずれも、再生骨の材料特性および力学特性の向上に効果を及ぼさないことが示唆された。先行研究[6]では、骨回復はまず量的回復が進み、それに遅れて骨の材料強度を決定するアパタイト結晶の配向が形成されると報告されている。欠損作製20日後ではアパタイト配向性も未発達で、材料特性,力学特性の回復に至らなかった可能性が考えられる。本研究において、骨量回復が有意に先行しているSham群とOVX-C群との間でも材料特性および力学特性の全パラメータに有意な差が認められなかったことは、このことを支持している。WBVあるいはiPTHが再生骨の成熟性を促進し、骨材料・力学特性の回復に寄与するのは、骨修復治癒後期のリモデリング過程においてであることが推測される。今後、さらに治癒が進行した再生骨試料を用いた検討が必要である。
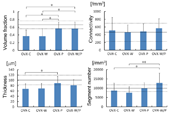
図2.CT計測による再生骨形態特性解析の結果。実線および破線はそれぞれSham群の平均値および平均値±標準偏差を表す。統計検定はTukey multiple comparison testによる多重比較検定により行った。検定の有意な差は*: P<0.05,**: P<0.01の二段階とした。

図3.FTIR-MSによる再生骨材料特性解析の結果。各々、骨ミネラル化,I型コラーゲン架橋度(成熟度),アパタイト結晶化の強度を示す。実線および破線はそれぞれSham群の平均値および平均値±標準偏差を表す。統計検定はTukey multiple comparison testによる多重検定により行った。

図4.ナノインデンテーションによる再生骨力学特性解析の結果。実線および破線はそれぞれSham群の平均値および平均値±標準偏差を表す。統計検定はTukey multiple comparison testによる多重比較検定により行った。
今後の課題:
本研究ではいずれの治療についても、再生骨の材料・力学特性に対して有意な効果を検出できなかったが、治療効果の発現は再生骨の成熟度に依存する。そのため、WBV,iPTH,およびWBVとiPTH併用治療については、より長期の治癒期間に渡って評価する必要があると考えられる。
参考文献:
[1] Slatkovska L. et al., Osteoporos Int 21 1969-1980 (2010).
[2] Leung K.S. et al., J Orthop Res 27 458-465 (2009).
[3] Sugiyama T. et al., Bone 43 238-248 (2008).
[4] Wehrle E. et al., Disease Models & Mechanisms 8 1-12 (2015).
[5] Yaser M. et al., J Bone Joint Surgery 87 731-741 (2005).
[6] Nakano T. et al., 生体医工学 44 503-510 (2006).
ⒸJASRI
(Received: March 19, 2015; Early edition: May 28, 2015; Accepted: June 29, 2015; Published: July 21, 2015)






