Volume1 No.2
Section B : Industrial Application Report
無機蛍光体の室温合成の実用化
Inorganic Phosphor Preparation at Room Temperature
a新潟大学超域学術院, b新潟大学自然科学研究科, c新潟大学工学部
aCenter for Transdiciplinary Research, Niigata University, bGraduate School of Science & Technology, Niigata University, cFaculty of Engineering, Niigata University
- Abstract
放射光を用いたXAFS分析にて、室温で原料を接触させて静置するだけで反応させたRbVO3:EuおよびCsVO3:Eu蛍光体の発光中心の価数評価を行った。Eu(ユウロピウム)を賦活したXANES領域の測定では、通常の固相反応法で合成された蛍光体と同等でいずれの試料もEuがすべて3価で存在する結果が得られ、固相反応法に変わるものと期待できることが確認された。
キーワード: RbVO3、CsVO3、蛍光体、XANES
背景と研究目的:
代表的なバナジン酸塩蛍光体であるYVO4:Eu3+は高輝度を示す赤色蛍光体であり、液晶ディスプレイのバックライトである冷陰極蛍光管(CCFL:Cold Cathode Fluorescent Lamp)やプラズマディスプレイなどに使用されている。また、CsおよびRbを含むバナジン酸塩CsVO3およびRbVO3は母体発光を示す高効率な蛍光体材料であることは既に報告されている[1,2]。
我々は、若干量の水分の存在下で原料である粉末Rb2CO3およびCs2CO3とV2O5を接触させるだけで粉末原料の間で固相反応が進行し、室温において結晶性のバナジン酸塩CsVO3およびRbVO3が得られることを見出した[3]。室温で加熱なしに結晶質の複合酸化物を合成することは非常に稀であり、報告が無いといってもよい。無機蛍光体は粉末で用いるため、本合成法のように粉末のまま生成物が得られるメリットは非常に大きい。加熱なしに複合酸化物ができれば、これまで使われていたガス炉・電気炉を用いずに合成できることから、プロセスの簡略化だけではなく飛躍的な省エネルギーのプロセスとなる。実用化に向けて発光色の多色化のためにさまざまな条件で試料を合成し、その物性を調査している。今回は、発光色多色化のために発光中心の状態(価数)がどのようになっているのか、基礎的な調査を目的としている。一般的に、蛍光灯用蛍光体などではEu3+,Eu2+,Tb3+が発光中心として使われており、LED用蛍光体ではCe3+が使われている。蛍光体の発光中心イオンの賦活濃度は、母体結晶中の構成元素に数mol%程度の量であり、通常の化学分析では難しい。また、実験室系のX線回折装置などでも母体結晶中に固溶しているかを見極めることも難しいため、低濃度の対象元素にも有効な分析手段[4,5]である放射光X線によるXAFS測定を行い、発光中心の価数の調査を行った。
実験:
蛍光体の発光色の多色化を行うために、希土類発光中心を導入した試料を作製する。作製条件によりこの試料の発光イオンの価数状態の差異を確認するために、CsVO3およびRbVO3にEuを賦活した試料のEuのXANESの測定をSPring-8のBL14B2で行った。なお、通常法との比較のため、500°C、1時間で焼成した通常固相法の試料を準備し、EuのXANESを測定した。試料は予め良く砕いて所定量の窒化ホウ素と混合してペレット状にしたものを透過法用に準備した。また、これとは別に粉末試料をポリエチレンバックに充填して蛍光法用の試料とした。実験では、先ずイオンチャンバーを使った透過法による測定を試みたが、吸収端のジャンプが十分に測定できなかったため、19素子半導体検出器を用いた蛍光法にて測定を行った。これにより時間の制約のため申請した試料のほとんどを再測定(複数回測定)することとなり、またTbは測定エネルギー域が離れていたため装置条件変更に時間がかかり、全ての試料を測定することができなかった。またCeを賦活した試料の測定では、Ce-LIII吸収端のXANES領域がV-K吸収端のEXAFS領域と重なり、解析に不十分な測定となった。
結果および考察:
試料は、Rb2CO3(またはCs2CO3)とV2O5を量論比で乾式混合し、20°Cの実験室内に24時間以上放置したものを使用した。放置中に空気中の水分を吸収し、RbVO3(またはCsVO3)へと変化する。この試料のX線回折の詳細な結果は、成果報告書(課題番号2011B1985)に詳細は譲るが、単相で合成できていることを確認した。また蛍光特性は、特開2011-16670に示すようなデータが得られており、400-700 nmの幅広の白色発光が観測されている。このような事前実験のデータを基に実験を行った。
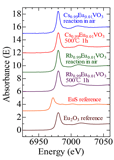
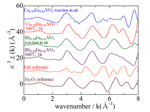
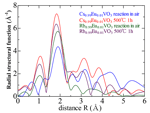
XANES測定による結果を図1に示す。Eu-LIII吸収端は6.98 keV付近にある。測定したデータを見ると、7.01 keV付近のピークにおいて、室温大気に放置した試料の方が電気炉焼成した試料に比べて、やや低エネルギー側に測定されているものの、CsVO3およびRbVO3にかかわらず、室温・大気中に放置して反応させた試料でも、電気炉・大気中500°Cで熱処理した試料でも、ほぼ同様のピークが観測された。図2に示すようにk3χの挙動は、どのCsVO3やRbVO3などの作製試料も波数5 Å-1程度まではほぼ同じであった。さらに詳しく見ると波数5 Å-1以上の領域でも500°C焼成の試料同士と本合成法で作製した試料同士は比較的類似していた。併せて、2 < κ < 8 Å-1のフーリエ変換により得られた動径構造関数(図3)のデータでも、第一近接の距離はどの試料も1.8 Å程度でありほぼ同じであったが、データの質が悪く、詳細な微細構造の解析をするに十分なデータが得られなかったが、これらのことから、本実験の試料作製法は、通常の固相法による焼結プロセスと比べて、賦活したEu周囲の局所的構造はほぼ同じと考えられる。
図1.CsVO3:Eu、RbVO3:EuのEu-LIII XANESスペクトル
(EuSはEu2+、Eu2O3はEu3+の参照試料)
図2.EXAFS領域の波数とk3χの算出結果
図3.CsVO3:Eu、RbVO3:Euの動径構造関数
Euは2+と3+の価数をとることができる。2価の基準物質であるEuSと3価の基準物質であるEu2O3と比較しても、作製試料の吸収端は3価であるEu2O3の吸収端と同じエネルギー位置にあり、作製試料中に含まれるEuは全てが3+であることが分かった。蛍光体としての発光強度とEuのLIII端のピークとの関連性は見られなかった。別途測定した発光スペクトルによれば、RbVO3(またはCsVO3)のVO4由来の発光が幅広なスペクトルで強力であった。Eu3+を添加した試料は、600-620 nm付近に肩が現れており、f-f遷移による発光も発現していると考えられるが、更なる詳細な実験が必要である。
今後の課題:
Euは3価での発光も示すが、2価での発光も興味深い。現在、添加する水分のpHを変化させるなど、合成条件と価数の変化についての関連性を調査できるよう検討しているところである。
参考文献:
[1] T. Nakajima et al., Nature Materials, 7, 735 - 740 (2008).
[2] M. Sayer: Phys. Stat. Sol. (a), 1, 269-277 (1970).
[3] 特開2011-16670
[4] 太田俊明編、X線吸収分光法、アイピーシー(2002).
[5] I. Hirosawa et al., J. SID., 12, 269 - 273(2004).
©JASRI
(Received: April 5, 2012; Accepted: March 8, 2013; Published: June 28, 2013)