Volume1 No.3
Section B : Industrial Application Report
Biドープリン酸塩ガラス中でのBi周りの配位構造解析
Coordination Structure around Bi Ion in Bi-doped Phosphate Glasses
a京都工芸繊維大学, b大阪大学, c龍谷大学, d五鈴精工硝子(株), e(特定非営利活動法人)レーザー技術推進センター, f(公財)高輝度光科学研究センター
aKyoto Institute of Technology, bOsaka University, cRyukoku University, dIsuzu Glass Co. Ltd., ePromotion center for Laser Technology, fJASRI
- Abstract
-
Bi(ビスマス)をドープしたガラスにおける可視光励起による近赤外域での発光の原因を調査するために、Biドープリン酸塩ガラスについて、Bi LIII吸収端でのXAFS測定を行った。また、比較のため、Biドープソーダ石灰ガラスについても測定を行った。XANESは、Bi濃度や溶融雰囲気の還元性の強さが異なってもほぼ同じで、Bi2O3結晶に近い形状を示した、またBiドープソーダ石灰ガラスも同じXANESであった。一方、EXAFSはリン酸塩ガラスとソーダ石灰ガラスは異なり、後者の方が前者に比べ、Bi2O3に近いスペクトルを示した。
キーワード: Biドープリン酸塩ガラス、XAFS、蛍光法、配位環境、近赤外発光
背景と研究目的:
2001年にFujimotoらにより、Biを少量含むシリカガラスにおいて1.3 μm帯を中心とする300 nm以上の広帯域で強い発光が見出されて以来[1]、この波長帯での広帯域、高効率光アンプへの応用を念頭にBiをドープした様々なガラス系の発光特性に関する研究が行われてきた[2]。一方、Biにおける発光中心に関する研究も、XAFSやESRなどの分光学的な分析手段を用いて検討がなされてきたが、十分には特定されていない。例えば、FujimotoはBiドープシリカガラスの発光中心について6配位のBi5+であると報告しているが[3]、Mengらによれば、Biドープアルミノリン酸ガラスにおける発光中心について、低原子価のビスマス、すなわちBi+やビスマスクラスターである可能性が高いと報告している[4]。
我々はこれまで、レーザー用ガラスとして多く用いられてきたリン酸塩系を中心に、ガラス組成と、Biに由来する吸収、蛍光などの分光特性との関係を調査してきた。そのなかで、ある特定の組成のBiドープリン酸塩ガラスにおいて、Biドープシリカガラスと同様に可視域に吸収が観察される(450 nm, 700 nm付近)こと、さらに、500 ~ 800 nmの範囲での励起により波長1.15 ~ 1.3 μmの近赤外域において蛍光が観察されることが明らかになった。また、蛍光強度は、Biドープシリカガラスの半分程度であった。一方、Biドープソーダ石灰ガラスでは蛍光は観察されなかった。
そこで、本研究では、Biの濃度および溶融雰囲気を変化させ作製したBiドープリン酸塩ガラスについて、Biイオンの酸化状態や配位環境などをX線吸収スペクトルで調査し、これによって得られるBiイオンのガラス中での化学的な存在状態に関する情報と、Biの濃度、作製条件およびBiによる吸収、発光特性との関係を明らかにすることを目的として実験を行った。
実験:
ベースガラスは60P2O5・8.5Al2O3・3.5B2O3・26CaO・2K2O(mol%)とし、これに外割でBi2O3を0.1, 0.3, 1.0, 3.0 mol%ドープしたガラスを作製した。Biのドープ量を変化させた理由は、発光に資するBiの化学種の割合が、溶融条件だけではなく濃度にも依存すると考えたからである。
ガラスの作製は、P2O5, Al2O3, B2O3, CaCO3, K2CO3を原料として、1350℃で1.5時間溶融し、融液を室温まで急冷し作製した。原料として用いるリン酸(P2O5)の一部をリン酸二水素アンモニウム(H2NH4PO4)に置き換えることによって溶融雰囲気の還元性を調整した。Bi2O3のドープ量が同じの試料についてそれぞれ還元雰囲気の異なる2種類のガラスを作製した。得られたガラスは、約10×10×5 mm3の板状に成形し、各面を光学研磨して測定用試料とした。また、比較のため、Biドープソーダ石灰ガラス(74SiO2・16Na2O・10CaO・1Bi2O3)も作製した。Bi2O3を3 mol%含む試料については、粉末試料も作製した。表1に作製したBiドープリン酸塩ガラスの外観を示す。H2NH4PO4添加量が同じ(0.4 mol%)試料(すなわち同程度の還元雰囲気で溶融)で比較するとBi2O3ドープ量が多いほど着色の濃いガラスが得られた。また、同じBi2O3ドープ量で比較した場合、より強い還元雰囲気で溶融したガラスほど着色は濃い。
XAFS測定は、SPring-8 BL14B2でSi(111)分光結晶を用い、Bi LIII吸収端について行った。測定は、上記のガラス試料および標準試料として、Bi金属、Bi2O3、NaBiO3の粉末試料について行った。粉末試料(標準結晶試料、およびBi2O3を3 mol%含むリン酸塩ガラス粉末)は、適切な濃度になるように窒化ホウ素粉末と混合し、ペレット成形した。ペレットについては、透過法で、板状ガラス試料については、19素子Ge半導体検出器を用いて蛍光法で測定を行った。
また、申請段階では、低温での近赤外域蛍光特性との対応を念頭に、1試料について低温での測定を計画していた。しかし、蛍光特性のデータがまだ得られておらず、また、もともと構造における不均一性が大きいアモルファス状態である試料の低温測定の意義についても再検討した結果、今回は行わなかった。
表1.作製したガラスとその外観.
ベースガラスの組成は60P2O5・8.5Al2O3・3.5B2O3・26CaO・2K2O(mol%)a).

結果および考察:
図1に、Bi2O3、Bi金属、NaBiO3およびBiドープリン酸塩ガラス、ソーダ石灰ガラスのBi LIII端XANESスペクトルを示す。Bi2O3、Bi金属、NaBiO3はそれぞれ特徴的なスペクトルを示した。
一方、Biドープガラスは、リン酸塩ガラス、ソーダ石灰ガラスいずれも、また、リン酸塩ガラスにおいてはBi2O3のドープ量に関わらず、ほぼ同様のスペクトル形状を示した。図にはすべてのスペクトルを示していないが、同じドープ量で溶融雰囲気の異なるリン酸塩ガラス(図中eとf)もそれぞれほぼ同様のスペクトルを示した。これらのスペクトルは、標準結晶の中では、Bi2O3結晶のスペクトルに最も近い。
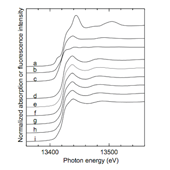
図1.結晶(a: NaBiO3, b: Bi2O3, c: Bi metal powder)および、Biドープガラス(d: 0.1 (0.4), e: 0.3 (0.8), f: 0.3 (0.4), g: 1.0 (0.4), and h: 3.0 (0.4) mol% Bi-doped phosphate glasses(( )内の数字はH2NH4PO4添加量(図2,3のキャプションも同じ)), i: 1.0 mol% Bi-doped soda-lime silicate glass)のBi LIII吸収端でのXANES.結晶は透過法にて、ガラスは蛍光法にて測定.fに比べeのガラスはより強い還元雰囲気で溶融されている.
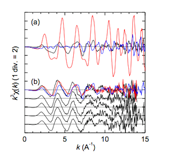
図2.(a) 結晶( ー : NaBiO3, ー : Bi2O3, ー : Bi metal powder)および、(b) Biドープガラス( ー : 上段より、0.1 (0.4), 0.3 (0.8), 0.3 (0.4), 1.0 (0.4), 3.0 (0.4) mol% Bi-doped phosphate glasses, 上段 ー 1.0 mol% Bi-doped soda-lime silicate glass, 上段 ー B2O3結晶)のBi LIII吸収端でのEXAFS振動スペクトル(k3χ(k)).結晶は透過法にて、ガラスは蛍光法にて測定.
図2に図1で示した試料のBi LIII端EXAFS(k3χ(k))振動スペクトルを示す。Bi2O3ドープリン酸塩ガラスは、いずれもほぼ同じEXAFSを示した。また、(b)の最上段の3つのスペクトルを比較すると、Biドープソーダ石灰ガラスは、Biドープリン酸塩ガラスと似たスペクトルを示したが、周期はB2O3結晶に近いことが分かる。
図3に図2をフーリエ変換したRSF(Radial structure function)を示す。なお、フーリエ変換の範囲は、NaBiO3結晶、Bi金属に対しては、それぞれ2〜18 Å-1、2〜17 Å-1、Bi2O3結晶、Biドープガラスに対しては3〜12 Å-1である。(a)のBi金属のRSFにおける3 Å付近のピークはBi – Biによる。NaBiO3, Bi2O3結晶における1.7 Å付近のピークはBi – Oに帰属される。Bi2O3結晶では、短距離側にショルダーが観察された。Bi2O3結晶(α-Bi2O3)では、概ねBiに対して2.2 Åと2.5〜2.6 Åの2種類の結合距離で酸素が配位していることから[5]、この2つが区別されている可能性があるが、今後、フーリエ変換の範囲も含めて慎重に検討する必要がある。また、3.5 Å付近にもピークが見られるが、これは第2配位圏にあるBiおよび酸化物に帰属される。一方、NaBiO3結晶では、Bi2O3に比べて大きなピークを示し、また、3.1 Å付近にもピークが見られた。(b)のBiドープガラスのRSFに見られる1 Å以下でのピークはゴーストである。Biドープリン酸塩ガラスでは、1.66 Å付近にピークが観察された。これは、Bi2O3やNaBiO3におけるピークに比べやや短い。ソーダ石灰ガラスではさらに短くなり1.60 Åとなった。
Bi2O3結晶、リン酸塩ガラス、およびソーダ石灰ガラスについて、Bi2O3結晶では1.013〜2.117 Åの範囲で、ガラスでは、0.921〜2.209 Åの範囲でフィルターをかけ逆フーリエ変換を行い、k3χ(k)を得た。図4に得られたk3χ(k)に対して、3〜12 Å-1の範囲でカーブフィッティングを行った結果の例を示す。Bi2O3結晶は、1-shellモデルでフィッティングした。また、位相シフトと後方散乱振幅は、FEFF8.2を用いてBi2O3結晶モデルについて行った計算値を用いた。表2にフィッティングで得た構造パラメータを示す。リン酸塩ガラス中では、Bi – Oの結合距離は、Bi2O3結晶のそれよりも長くなり、また、ソーダ石灰ガラス中では短くなった。Bi2O3結晶とリン酸塩ガラス中での結合距離が、図3で示したRSFのピーク位置と逆になったのは、Bi2O3結晶について1-shellモデルでフィッティングしたためであると考えられる。Bi2O3結晶について、配位数が小さく出ている点、またガラスにおいてもその可能性がある点については、検討を行っている。
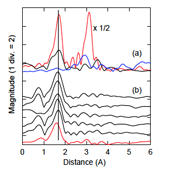
図3.(a) 結晶( ー : NaBiO3, ー : Bi2O3, ー : Bi metal powder)および、(b) Biドープガラス(上段より、0.1 (0.4), 0.3 (0.8), 0.3 (0.4), 1.0 (0.4), 3.0 (0.4) mol% Bi-doped phosphate glasses, ー 最下段 1.0 mol% Bi-doped soda-lime silicate glass)のBi LIII吸収端でのRSF (Radial structure function).
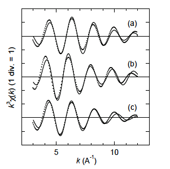
図4.カーブフィッティング結果(例)(a) Bi2O3結晶 (b) Biドープリン酸塩ガラス(Bi2O3ドープ量 1.0 mol%, H2NH4PO4添加量 0.4 mol%)(c) Biドープソーダ石灰ガラス.実線:実験値、点線:フィッティング.
表2.カーブフィッティングの結果
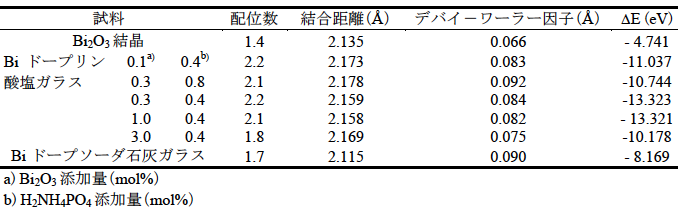
表2および図1のXANESスペクトルより、リン酸塩ガラス中でのBiの配位環境はBi2O3ドープ量、溶融条件の違いによらず大きな差は認められず、ソーダ石灰ガラス中のBiの配位環境とともに、Bi2O3に近いと考えられる。また、Bi – Oの結合距離は、リン酸塩ガラス中の方が、ソーダ石灰ガラス中に比べてやや長い。このような距離の違いに対する原因として、それぞれのガラスを構成するネットワーク構造の違いが考えられる。ソーダ石灰ガラスは、SiO4四面体が頂点を共有したネットワーク構造を形成しており、そこにNa2OやCaOなどのガラス修飾酸化物が導入されることによって非架橋酸素が形成され、それに伴って随所にネットワークが切断された構造を持つことはよく知られている。
一方、本研究で調査したリン酸塩ガラス(より正確にはアルミノボロリン酸塩ガラス)では、リン酸がO = PO3 – を単位としてネットワークを形成しており、Al2O3やB2O3は既に述べたようにO = P二重結合を開裂してPO4四面体と頂点を共有することにより四面体ネットワークを形成すると考えられる。またCaOやK2Oはケイ酸塩ガラスにおけるガラス修飾剤と同様に非架橋酸素を形成すると考えられる。このようなガラスネットワークを考えたとき、第1近似としてガラス形成酸化物に対するガラス修飾酸化物の割合が重要となる。本研究で用いたソーダ石灰ガラスでは、74 mol%のSiO2に対して26 mol%の(CaO, Na2O)が含まれる。一方、リン酸塩ガラスでは、72 mol%の(P2O5, Al2O3, B2O3)に対して28 mol%の(CaO, K2O)が含まれることになる。P2O5, Al2O3, B2O3はいずれもカチオンが2つ含まれているので、ガラス修飾酸化物の割合はソーダ石灰ガラスに比べて約1/2になる。ガラス修飾酸化物が多いほどネットワーク構造のフレキシビリティは大きくなる。もしこのようなガラスネットワークにBiが導入された場合、フレキシビリティが大きいネットワーク(ここではソーダ石灰ガラス)に導入された方がよりO2-を引きつけやすいと考えられる。このこともBi – O結合距離の違いの原因になっていると考えられる。
今後の課題:
今回の測定では、リン酸塩ガラスにおいてBiのドープ量や溶融雰囲気を変化させて作製し、着色が大きく異なるいくつかのガラスを作製した。これらのガラスは、近赤外域での発光強度も異なることが分かっている。しかし、これまでの解析では、XANES、EXAFSともに大きな違いは認められなかった。このことは、発光や着色の原因となるBiとXAFSで観察しているリン酸塩ガラス中に存在している大部分のBiが異なることを示唆している。一方、Biドープソーダ石灰ガラスはリン酸塩ガラスと異なったXAFSを示し、さらに蛍光は観察されない。このことより、ガラス組成が異なればBiの配位環境も異なり、このことが発光特性にも影響を与えていることは示唆される。
今後の課題として、より低濃度のBiドープリン酸塩ガラスにおいて十分な還元雰囲気で溶融することにより、発光に資するBiの割合を増加することができれば、XAFSスペクトルにおいても違いが検出できる可能性を検討する必要はあると考えられる。
参考文献:
[1] Y. Fujimoto, et al., Jpn. J. Appl. Phys., 40 [3B], L279 (2001).
[2] 例えば、V. V. Dvoyrin, O. I. Medvedkov, V. M. Mashinsky, A. A. Umnikov, A. N. Guryanov and E. M. Dianov, Opt. Exp., 16 (21), 16971.
[3] Y. Fujimoto, J. Am. Ceram. Soc., 93, 581 (2010).
[4] X. Meng, J. Qiu, M. Peng, D. Chen, Q. Zhao, X. Jiang and C. Zhu, Opt. Exp., 13 (5), 1628.
[5] H. A. Harwig, Z. Anorg, Allg. Chem., 444, 151 (1978).
ⒸJASRI
(Received: May 7, 2012; Accepted: November 1, 2013; Published: December 10, 2013)






