Volume8 No.1
SPring-8 Section A: Scientific Research Report
高エネルギーX線を用いたリコピン微結晶の単結晶構造解析
Single Crystal Analysis of Micro-Crystalline Lycopene by High-Energy X-ray
滋賀県立大学
University of Shiga Prefecture
- Abstract
-
トマトに含まれる色素のオール trans 型リコピンの微結晶を作成し、BL02B1 ラインで高エネルギーX線照射による単結晶構造解析を行った。ディスオーダーした分子構造が見られ、R 値は 13% 台になった。分子中の11個の連続するポリエン鎖は、メチル基の立体反発を示すように湾曲しており、また完全な平面でなくねじれた構造をしていることが明らかになった。結晶構造において、分子はポリエン鎖が π-スタッキング相互作用を行うように配置しており、固体状態において光分解しやすい実験事実が裏付けられた。
Keywords: リコピン、分子構造、結晶構造
背景と研究目的:
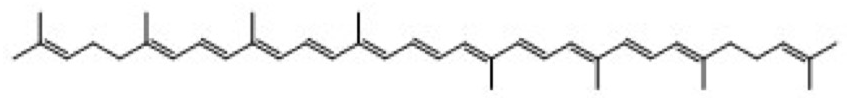
トマトに含まれる色素リコピン(分子構造式を図1に示す)は、カロテノイドと呼ばれる天然物の一種である。リコピンは野菜や果物の中で色素として存在しているだけでなく非常に高い抗酸化能を有しており、その一重項酸素消去能は他のカロテノイドと比較しても非常に高い値を示すことがわかったなど、一重項酸素が原因とされている癌や糖尿病、高血圧などの生活習慣病の予防に有効な化合物として近年非常に注目されている[1]。リコピンは C40H56 からなる組成式を持つ分子であり、生合成された直後のものは単結合と二重結合が交互に並んだ部分が全てトランス配座である(分子の中央部に11個の共役二重結合が存在し、これらの二重結合に結合した置換基が全て二重結合の反対側にある E 配置をとっているので、立体化学を厳密に扱う場合は(all-E)リコピンと呼称する)が、光または熱によるトランスからシスへ異性化しやすいことおよび構造変化により腸内吸収性や一重項酸素消去能の向上が見られることが最近見出されてた。我々の研究室では、これまでに単離されてこなかったリコピン異性体の混合物からの分離方法の探索とそれぞれの異性体の化学的および物理的性質の調査を行っている。近年、リコピンは社会的な知名度が高く注目されている物質の1つであるが、その分子構造という基本的な事項でさえも実験的に明らかにされていない。単結晶作成および化合物の扱いの困難さのため、カロテノイドでX線結晶構造が報告されている例はわずかである。例えば、同じカルテノイドに属するβ-カロテンのX線構造解析[2]が報告されているが、分子の末端に6員環構造をもち安定な構造を有している。これに対して、リコピンは鎖状構造をとり、分子内に多くの炭素-炭素単結合をもつことから、分子の構造の自由度が高く単結晶がそもそも作りにくいことが知られていた。我々は高純度リコピンの精製法を新たに開発し、結晶化の条件を種々検討していたところ、微粉末でなく針状の微小結晶を得る条件を見出した。しかし太さが 20 µm 程度と細く、通常の単結晶X線回折装置を用いる測定は困難であった。そこで、SPring-8 の高エネルギーX線を用いてX線回折を行い、構造解析を実行し、リコピン結晶の構造情報の取得を目的とした。
図1.リコピンの化学構造式
実験:
既報[3]により精製したリコピン(純度 99.3%)の粉末をジクロロメタンに溶解後、貧溶媒のアセトニトリルをゆっくり加え、遮光しながら2~3日間室温で放置すると、(all-E)リコピンの濃赤色の針状結晶を得ることに成功した(図2)。この結晶は −80℃ の冷凍庫で保存しておいても1か月ほどで退色していくため保存は困難である。このため、マシンタイムから逆算して結晶作成を行う必要があった。リコピン結晶を保冷しながら、BL02B1ビームラインに運び入れ、X線回折計(CCD-MERCURY)で測定を行った(X線波長 λ = 0.6999 Å)。測定に用いた結晶は 0.60×0.05×0.015 mm3 のものを選んだ。結晶の損傷を最小限にするため、90 K の温度設定、χ = 45°、ω スキャン(ω = 0~180°, 2°ステップ, ϕ= 0, 180, 90°, 合計 270 枚の振動写真)で計測した。204631 点の反射を計測し、その内独立した反射の 7457 点を解析に用いた。構造解析ソフトウェアパッケージ WinGX[4]を用い、直接法に SIR2004[5]、精密化に SHELX2013[6]を用い解析を行った。リコピンの片側の末端において 0.494(7):0.506(7)のディスオーダーのモデルを組んで精密化を収束させた。水素原子は riding atom で扱った。結晶データは以下の通りになった:monoclinic, C2/c, a=65.893(18)Å, b=6.1572(16)Å, c=16.851(5)Å, β=96.040(7)°, V=2799(3)Å3, dcalc=1.049 Mg/m3, Z=8, R1 [I >2σ(I )]=0.1316, wR2 (all)=0.3899, GOF=1.035。
図2.リコピンの単結晶
結果および考察:
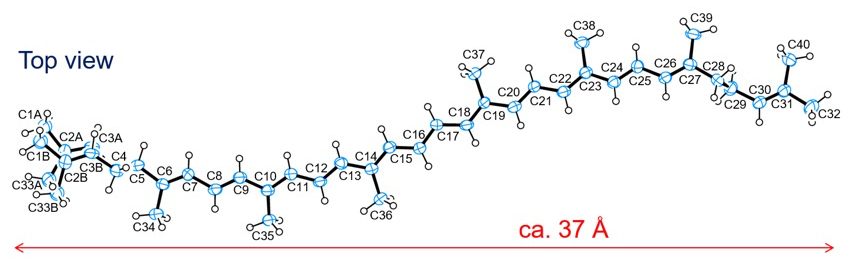
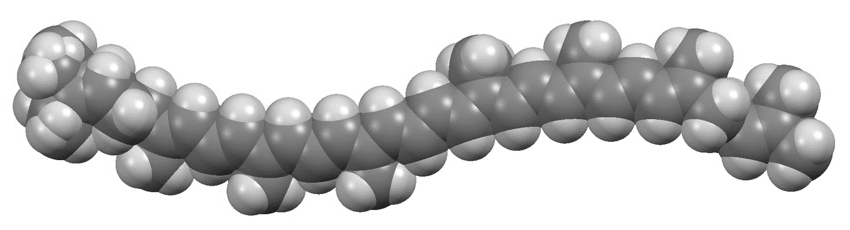
X線の連続照射でリコピンが壊れていくことが回折像から判断されたので、露光時間を少し短めに設定する必要があった。分子構造の ORTEP 図を図3に示す。全長が約 37 Å の分子であることがわかった。分子の左末端の温度因子が右末端より大きいことは乱れ構造(ディスオーダー)と関係していると考えられる。リコピン分子中には11個の二重結合を含むポリエン鎖が存在しており、all-trans 配座をとっていることが確認された。このポリエン鎖は、側鎖のメチル基の立体反発の存在のため湾曲しており、また、ポリエン鎖は完全な平面でなくねじれた構造をしていることが明らかになった。CPK モデル図(図4)から分子全体は「いも虫」を連想させる形状をとることがわかった。
図3.リコピンの ORTEP 図
図4.リコピンの CPK モデル図
さらに、天然のトマトの色は色褪せることはないが、固体状態のリコピンが冷凍保存でも退色していく事実は、固体中における分子の配列が退色を行う何らかの化学反応に関係していることが考えられた。そこで、結晶構造における分子配列を注意深く観察した。結晶全体の構造を図5に示す。分子は、平行に配列し、図の垂直方向からは斜めにずれて積み重なっている様子がうかがえた。
図5.リコピンの結晶構造(b軸投影図)
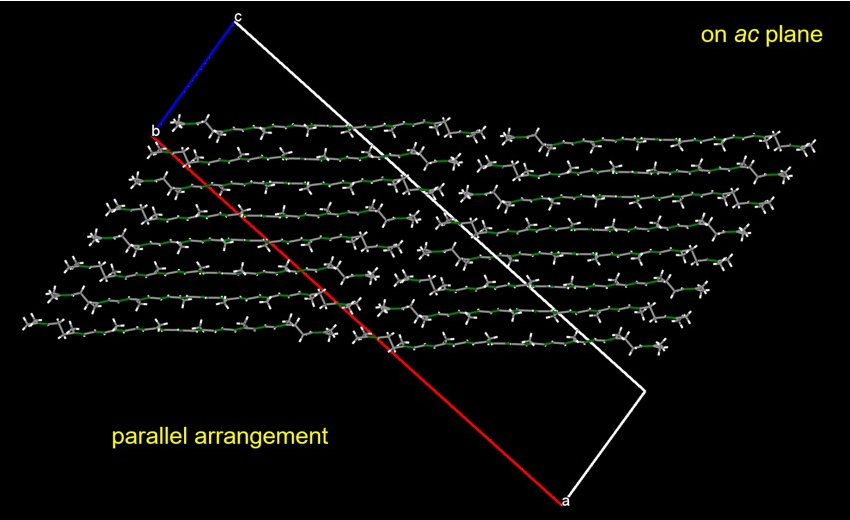
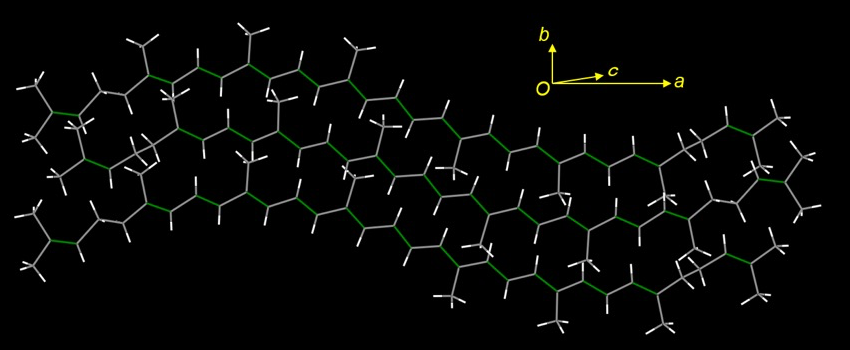
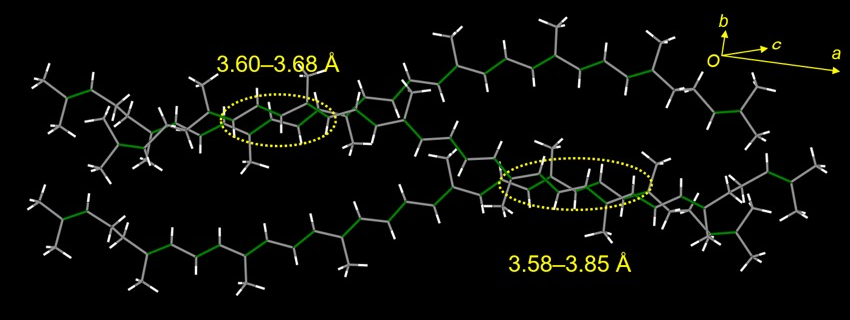
また、積み重なり方に特徴があるかを調べると、2通りの配列の違いがあることがわかった(図6と7)。すなわち、一つは分子が同じ向きに並ぶ詰まり方(図6)で、もう一つは分子が交差して並ぶ詰まり方(図7)である。後者においては、sp2 混成軌道の炭素原子間の距離が 3.6~3.8 Å と短く、固体状態でも反応が起こりやすい可能性を示唆している。固体状態でリコピンが退色を行うメカニズムとして、光や酸素が存在すると隣合うリコピン間で重合反応が起こり、ポリエン鎖が短くなり、共役系が短くなり退色が起こること考えられる。
図6.リコピンの積み重なり その1
図7.リコピンの積み重なり その2
今後の課題:
天然のカロテノイド分子において、X線結晶構造解析が行われた例は極めて少ない。リコピンもその一つであるが、単結晶を得ることの難しさと固体状態での安定性が意外にも低いことが、構造決定の分野での進展を遅らせる要因となっていることが考えられた。できるだけ質の優れた結晶をスケジュールに合わせて作り出す技術を完成させることがX線結晶構造解析において重要であり、リコピンはその扱いが難しい部類の物質と言える。リコピンと何かを反応させ安定な複合体を形成させて、その複合体の構造を調べるといったことを行わないと、リコピンの精度のよい結果が得られにくいと考えられる。
参考文献:
[1] P. D. Mascio, S. Kaiser, H. Sies, Arch. Biochem. Biophys., 274, 532 (1989).
[2] H. Hashimoto et al., Jpn. J. Appl. Phys., 37, 1911 (1998).
[3] M. Takehara et al., J. Agric. Food Chem., 62, 264 (2014).
[4] L. J. Farrugia, J. Appl. Crystallogr., 32, 837 (1999).
[5] M. C. Burla et al., J. Appl. Crystallogr., 38, 381 (2005).
[6] G. M. Sheldrick, Acta Crystallogr. A, 64, 112 (2008).
(Received: September 30, 2019; Early edition: November 28, 2019; Accepted: December 16, 2019; Published: January 22, 2020)