Volume7 No.1
SPring-8 Section B: Industrial Application Report
Ag含有ゼオライト蛍光体の実用化のための局所構造解析
― 水中におけるAg交換X型ゼオライトのAg局所構造 ―
Local Structure Analysis for Practical Use of Ag-containing Zeolite Phosphors
– Local Structure around Ag for Ag-exchanged X-type Zeolite in Water –
a山梨大学, bレンゴー株式会社中央研究所
a University of Yamanashi, b Rengo Co., Ltd.
- Abstract
-
Ag+ 交換した種々のゼオライトの、蛍光を示す調製条件と示さないものの Ag K 吸収端EXAFSを測定した。それらのうち、水中でも蛍光を発する Ag+ 交換したX型ゼオライトについて、水中での Ag の局所構造を解析した。Ag の含有量や交換後の処理温度を変化させると蛍光スペクトルの高さは変化したが、ピークの形や位置はほとんど変化しなかった。一方、EXAFSの解析によるフーリエ変換について、強度はいくらか変化するが形はほぼ変わらず、カーブフィッティング解析した局所構造も処理温度の違いによる変化がまったくなかった。
Keywords:Ag 交換ゼオライト、蛍光体、EXAFS
背景と研究目的:
Ag+ で交換したゼオライトは、加熱により蛍光を呈するようになることが古くから知られている[1]。これらの発光機構については、様々な研究が行われてきており、種々の電荷を持つ様々な大きさの銀クラスターを発光中心とする考えが主流である。これまでの研究で扱われてきたゼオライトは、ほぼ 100 % まで Ag+ にイオン交換したA型を真空中で数 100°C で加熱したものがおもな対象であり、それを空気に暴露するなどして酸素や水分を吸収すると発光しないものが多かった。この消光特性もクラスターを発光中心とする説の根拠の一つであった。しかしながら、貴金属クラスターの発光は種々観測され[2]、一方でゼオライト中でのクラスター生成も確認されている[1]ものの、ゼオライト中のクラスターと発光機構の関係は確定的な実験的証拠に乏しく、そのような機構を否定する報告[3]もある。これら蛍光を示すゼオライト中のクラスターの生成について確認するため、EXAFS(Extended X-ray Absorption Fine Structure; 広域X線吸収微細構造)による解析も行われてきている[4]。
ところが近年、種々のゼオライトを 20 % 程度の低い交換率まで Ag+ に交換した Ag 交換ゼオライトが、空気中での加熱によっても、空気中で長期間安定的に蛍光を発生することがわかってきた[5]。このような Ag 交換ゼオライトは、ゼオライトの種類や反応後の処理温度、あるいは Ag+ に追加して交換するイオンの種類などにより、さまざまな発光色を示すことから、蛍光材料としての実用性も検討されてきている。このように低い交換率ではクラスターはより生成しにくいと思われる。そのため、これらの系での蛍光の発光機構に対する基礎的な関心に加えて実用的な観点からも、ゼオライト中の Ag の状態を明らかにすることが重要である。そこで、本課題では種々のゼオライトを Ag+ とイオン交換し、さまざまな蛍光特性を示す条件により調製した試料のAg K吸収端X線吸収スペクトルを測定し、その解析を行った。
また、X型のゼオライトを使用すると、Ag 交換ゼオライトは交換反応後の水溶液に浸かったまま数 10°C に加熱するだけで容易に蛍光を示すことがさらにわかった。このように低い Ag+ 交換率のゼオライトを水中で加熱した場合には銀クラスターの生成はより考えにくいことから、これらの試料の Ag 周囲の局所構造をAg K吸収端のEXAFS解析により調べた結果について詳細に報告する。
実験と解析:
乾燥状態の試料の調製には、各ゼオライトのNa形を交換反応に用いた。Ag+ ならびに NH4+、Zn2+、Mg2+、あるいは Ca2+ を、用いたゼオライトの総イオン交換容量に対して図1から3に示した当量を含む水溶液を同時に加え、ゼオライトをイオン交換させた。いずれのゼオライトでも Ag+ に対する交換反応の選択性が非常に高いため、加えた Ag+ のほとんどが反応後にゼオライトに取り込まれたと考えられるが、他のイオンは加えた量よりも明らかに低い交換率になっているはずである。室温にて 24 h 反応後ガラスろ紙にてろ別し、所定の温度で加熱処理を行った。
水溶液中での蛍光を調べる試料のイオン交換反応には、東ソー社製F-9粉末ゼオライト原料を使用した。このゼオライト粉末については、組成分析で Si/Al モル比を確認し、粉末X線回折によりフォージャサイトのパターンが得られたことから、X型ゼオライトであることを確認した。そのまま反応させると Ag+ 交換反応時に微量の Ag2O を生成することがあるため、いったん純水で洗浄し乾燥したものを交換反応に使用した。ゼオライトに所定濃度の AgNO3 と 10 mmol/L の NaNO3 を含む水溶液を加え、25°C で 1 h 撹拌しイオン交換させ、ゼオライト中のAgの含有量が 0.5 mmol/g、1 mmol/g、2 mmol/g となる3種類の Ag 交換ゼオライトを調製した。なお、原料となるX型ゼオライト中の Na 含有量は 4.73 mmol/g であったので、実際の交換率は含有量が少ない方からそれぞれ約 11 %、21 %、ならびに 42 % となる。これら Ag 交換ゼオライトをそれぞれ3分割し、反応後の水溶液中で室温放置あるいは 70°C または 90°C で 24 h 加熱し放冷した。
これらの Ag 交換ゼオライトの、乾燥試料は錠剤に成型し測定に使用した。反応溶液と共存した状態の試料は、ホルダーに固定したポリ袋中に反応溶液とともに入れ、十分沈降した後に測定に使用した。Ag K 吸収端X線吸収スペクトルの測定を、BL01B1において透過法により行った。溶液と共存した試料の測定は、試料調製後約2週間後であった。測定は、Si(311)分光結晶を用いたクイックスキャンにより行い、測定したスペクトルの2回あるいは3回分を積算した。参照試料として、銀箔、Ag2O 粉末、ならびに AgAlO2 の測定も同様に行った。
X線吸収スペクトルからのEXAFS振動 χ(k)の抽出とフーリエ変換は、Xanadu[6]により行った。後の図に示したフーリエ変換はいずれも k = 2.0 – 12.2 Å−1 の範囲を用いており、吸収原子 Ag と散乱原子を O として位相シフトと後方散乱能の補正を行っている。カーブフィッティングによる解析は、フーリエフィルターを通さない χ(k)に対してDemeterのFeffit[7]を使用して行った。Feff計算では、Ag+ 交換したA型ゼオライトの結晶構造[8]を元に、A型の酸素8員環中に位置する Ag を Na に置き換え、最も Ag の占有率が大きい酸素6員環中心に位置する Ag を中心原子とした構造モデルを使用した。カーブフィッティングは χ(k) に対して k3 の重みをかけ k 空間において k = 2.5 – 12.2 Å−1 の範囲で行った。吸収端シフト ΔE0 は −8.118 eV で一定とし、O(2種類)、Si、Al の配位数は同じ値になるように制限し、0.5 mmol/g の含有量で 70°C 処理の場合に3となるように相対値として求め、Ag の配位数は最適化した。
XAFS測定後の反応溶液と共存した状態の試料の蛍光スペクトルの測定は、試料を反応溶液とともに石英製三角セルに詰め、粉末が十分沈降したのちに実施した。測定は日本分光製FP-6300により、励起光波長 320 nm、励起バンド幅 2.5 nm、蛍光バンド幅 5 nmの 条件で行った。この蛍光スペクトルの測定は、XAFS測定後1週間以内であった。
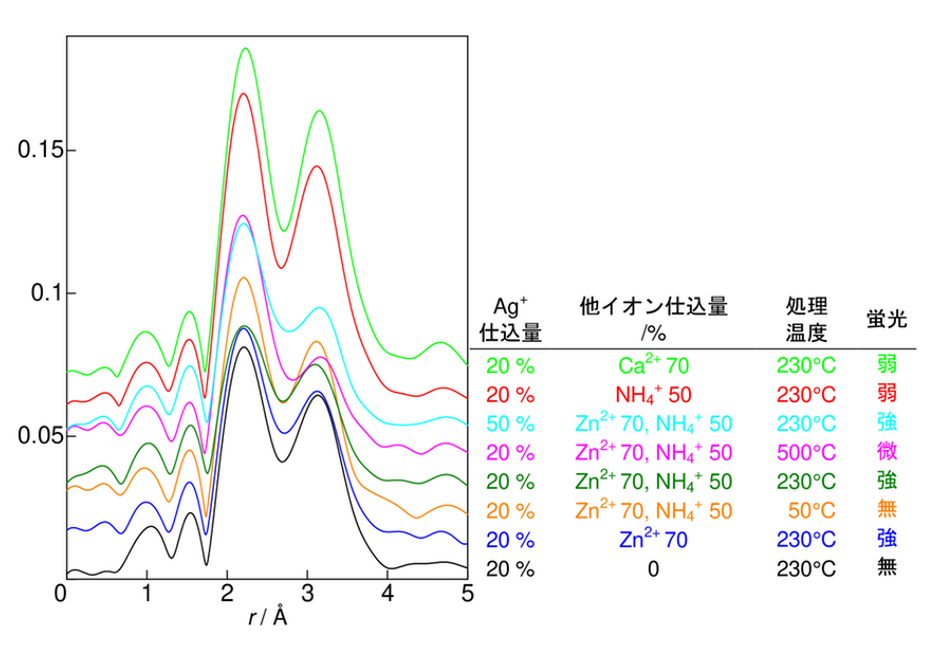
図1. 熱処理後の Ag 交換A型ゼオライトの Ag K 吸収端EXAFSフーリエ変換。Ag+ や他のイオンの仕込量(イオン交換反応に加えた量)は、使用したゼオライトの全イオン交換容量に対するイオンの当量比を示す。
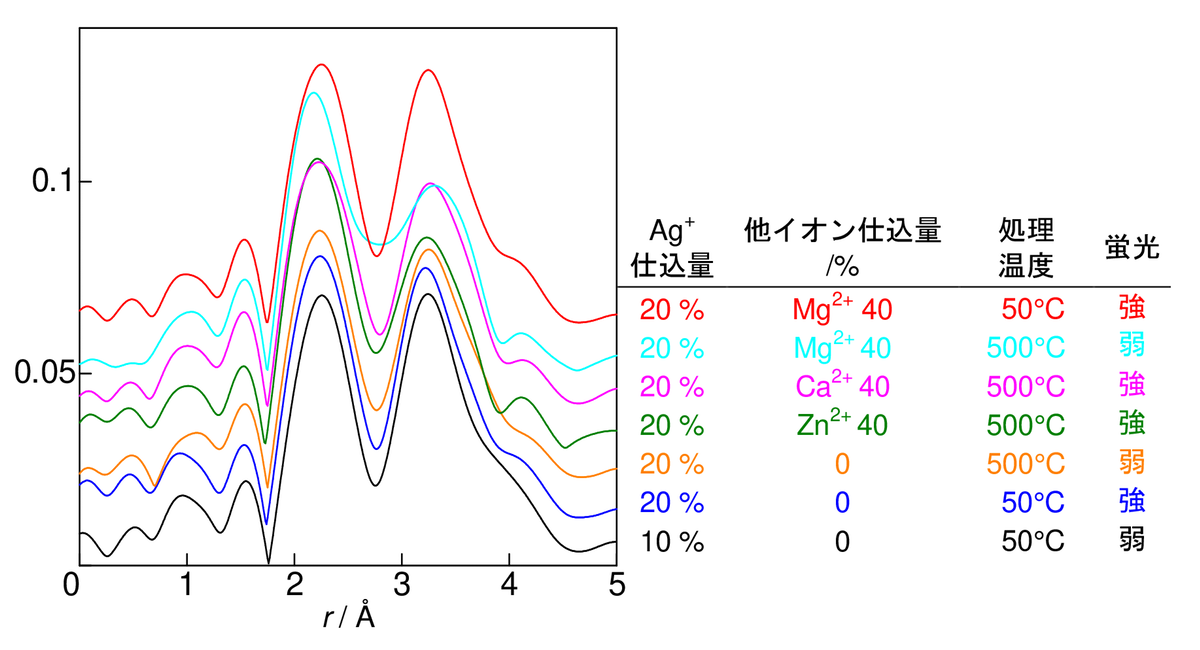
図2. 熱処理後の Ag 交換X型ゼオライトの Ag K 吸収端EXAFSフーリエ変換。Ag+ や他のイオンの仕込量(イオン交換反応に加えた量)は、使用したゼオライトの全イオン交換容量に対するイオンの当量比を示す。
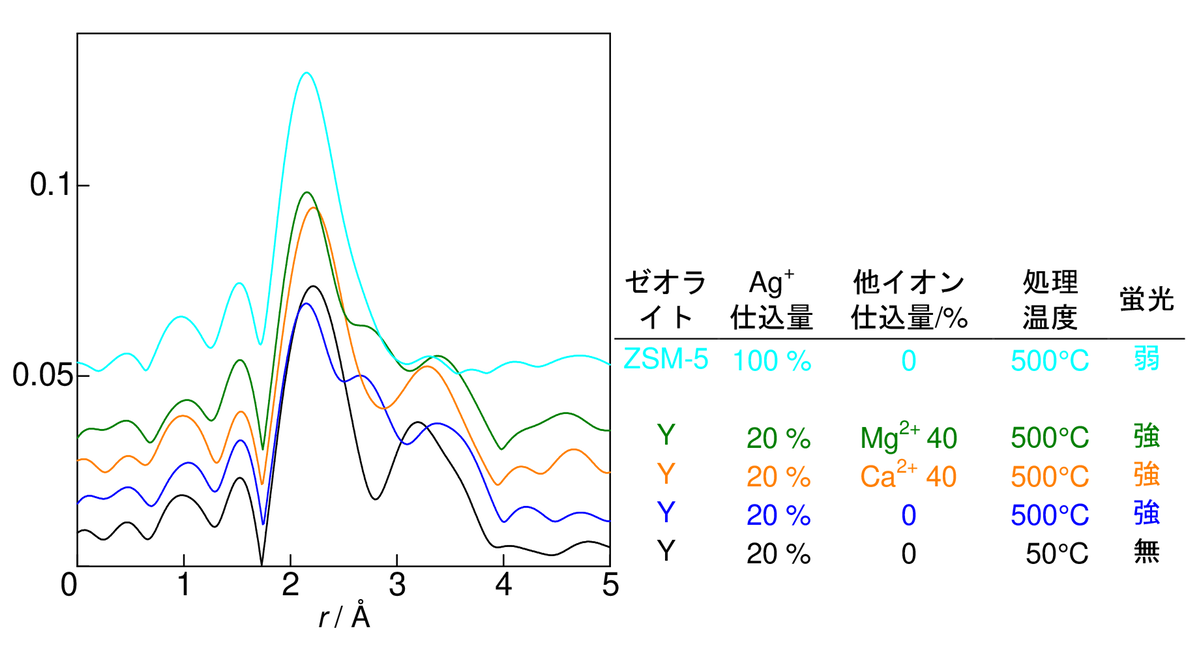
図3. 熱処理後の Ag 交換Y型、ZSM-5ゼオライトの Ag K 吸収端EXAFSフーリエ変換。Ag+ や他のイオンの仕込量(イオン交換反応に加えた量)は、使用したゼオライトの全イオン交換容量に対する加えたイオンの当量比を示す。
結果と考察:
図1から3に、乾燥状態の各種 Ag 交換ゼオライトのいくつかの試料のEXAFSフーリエ変換を示した。ほとんどが主として2本のピークを示すが、3本と見られるものもあり、一方ZSM-5では1本しか見られない。類似した調製条件の試料を比べると、それらの中で最も強い蛍光を示す試料でEXAFS信号が弱くなる傾向が見られるものの、処理温度が低すぎあるいは高すぎて蛍光が見られない試料でも大きな変化はなく、蛍光特性とEXAFSの間には明確な関連は見られない。Ag 以外に導入したイオンの有無や種類(ない場合には Na+ がケージ中に共存)の違いによってもはっきりとした違いはなく、ケージ中に共存するイオンの信号はEXAFSにはほとんど表れていないものと考えられる。特に2番目のピークが見られないZSM-5においても蛍光を示したことから、Ag と他の Ag やそのほかの共存陽イオンとの相互作用は、蛍光の発光機構に不可欠な条件ではないと思われる。
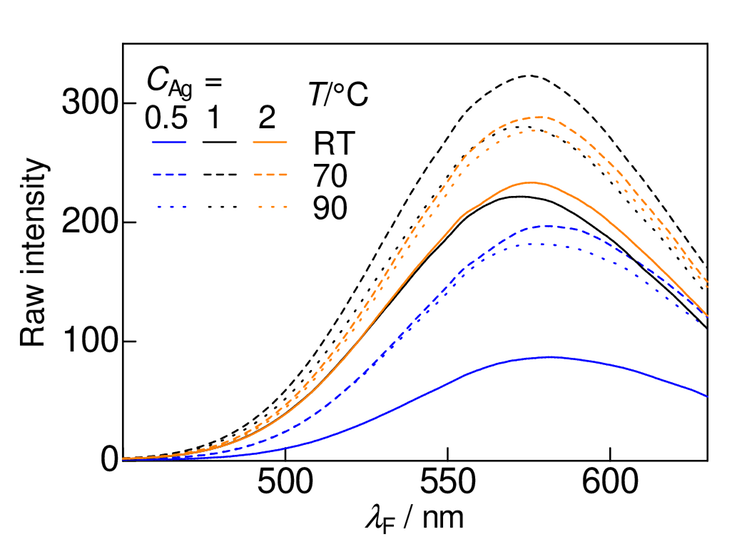
水溶液中で加熱した Ag 交換ゼオライトの蛍光スペクトルを図4に示す。蛍光ピークの高さは、Ag の含有量と処理温度により変化するが、いずれの条件でもスペクトルの形やピーク位置はあまり変化していない。同じ条件で調製した別の試料の実験では、イオン交換反応から 1 h 後ではわずかな蛍光しか観察されないが、室温のままでもさらに 1 h 経過した後には蛍光ピークが現れ、1週間後には強度が増加した。図4においても室温でXAFS測定まで約2週間、その後約1週間の計3週間程度放置されただけで、蛍光が観察されている。Ag の含有量が 1 mmol/g のものが最も強度が高く、Agが多いほど強いということではないことがわかる。またいずれの含有量でも 70°C で加熱した場合が最も高く、あまり高い温度は適当ではないことを示している。
図4. Ag交換X型ゼオライトの水中での熱処理後の蛍光スペクトル。励起光波長 320 nm。Ag 含有量 CAg は mmol/g 単位で、処理温度 T のRTは室温を示す。
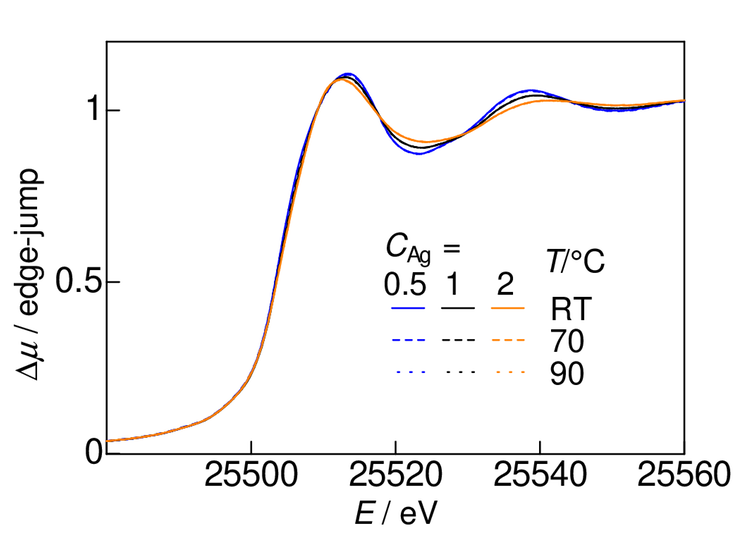
水溶液中の Ag 交換ゼオライトの Ag K 吸収端XANESスペクトルを、図5に示す。わずかに差が見られるが、これらの差は後に示すEXAFSの違いの延長でよく説明できるものであり、XANESとしての違いは見られない。乾燥試料でも同様にEXAFSの延長で解釈できるXANESの変化が見られた。これらは、Ag K 吸収端のエネルギーが高いことから、K殻空孔の寿命が短いことにより、また分光器の分解能が低下することにより、細かいXANESが見えなくなっているためと思われる。
図5. Ag 交換X型ゼオライトの水中での熱処理後の Ag K 吸収端XANESスペクトル。Ag 含有量 CAg は mmol/g 単位で、処理温度 T のRTは室温を示す。
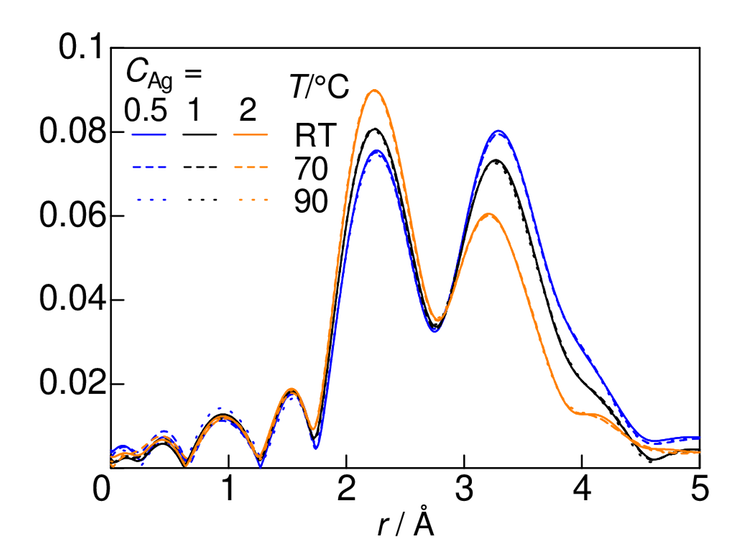
図5の試料の Ag K 吸収端EXAFSのフーリエ変換を図6に示す。いずれも r = 2.2 – 2.3 Å に現れている第1ピークと、r = 3.2 – 3.3 Å に現れている第2ピークの2本のピークが見られる。これらは図2に示した乾燥試料のものとも類似している。交換後の反応溶液と共存した状態であるが、反応後は溶液中の Ag+ の濃度は非常に低く、さらに光路内にある溶液の体積はゼオライトよりもかなり小さいため、水溶液中の Ag+ の信号は無視できる。
図6. Ag 交換X型ゼオライトの水中での熱処理後の Ag K 吸収端EXAFSフーリエ変換。Ag 含有量 CAg は mmol/g 単位で、処理温度 T のRTは室温を示す。
第1ピークは Ag に最も近いゼオライトケージの O を示すことから、この Ag-O 間距離を基に第2ピークを帰属すると、ゼオライト骨格の Si または Al、第2近接の O、あるいは Ag クラスターが生成している場合にはクラスター内の Ag-Ag、さらには交換されずにケージ中に残っている Na の可能性が考えられる。ここで、第1ピークでは図に示したフーリエ変換の絶対値と示していない虚部のピーク位置がほぼ一致していたのに対し、第2ピークではまったく合わなかった。一方、後方散乱能の補正の元素の設定を変えてフーリエ変換すると、O 以外のいずれの元素でも絶対値と虚部のピーク位置が第2ピークの位置にかなり近づく結果が得られた。これらのことから、第2ピークには O の信号はあまり含まれていないと考えられる。さらに乾燥試料ではケージ中の共存イオンの特徴による変化が見られなかったことから、第2ピークには Na+ の信号も寄与は小さいと考えられる。
Ag の含有量が増えると、第1ピークが高くなり第2ピークは低くなる一方で、温度による変化はまったく見られない。図4に示したようにこれらの調製条件を変えることで蛍光強度は大きく変化するが、仮にクラスターの生成の有無やその変化が認められるとしても、その局所構造は蛍光強度にほとんど無関係である。さらに Ag の含有量が少ない方の第2ピークが大きいことも、クラスター生成を考えると一見矛盾する。したがって、試料調製条件のことも考慮すると、クラスターの生成にはかなり疑問があると考えられる。
銀の含有量が 0.5 mmol/g で 70°C で処理した試料の、EXAFSカーブフィッティングを行った時の k3χ(k)を図7に示す。クイックスキャンで測定したことから、各点での積算時間が同じであるため、k が大きい領域で短周期のノイズが激しいように見られる。しかし、フィッティングの残差のフーリエ変換では、不一致のおもな成分は r = 2 Å 以下と 6 Å 付近に現れていることから、ある程度意味のある収束が行えているものと考えている。実験値、計算値はともに k = 6 Å-1 を境に振幅が急激に減少している。この振幅の減少は Ag 交換ゼオライトのほとんどに見られた。計算値を成分ごとに確認すると、それぞれの成分の振幅はなだらかに減少していくのであるが、k = 6 – 7.5 Å−1 の付近の範囲で各成分が互いに打ち消し合う波となっている。実験値もそのような振幅の変化を示すことで、この領域以降の χ(k)の抽出が多少困難になっている。
図7. Ag 交換X型ゼオライトの水中での熱処理後の Ag K 吸収端EXAFSの k3χ(k)とそのカーブフィッティング結果。Ag 含有量 0.5 mmol/g、処理温度 70°C。
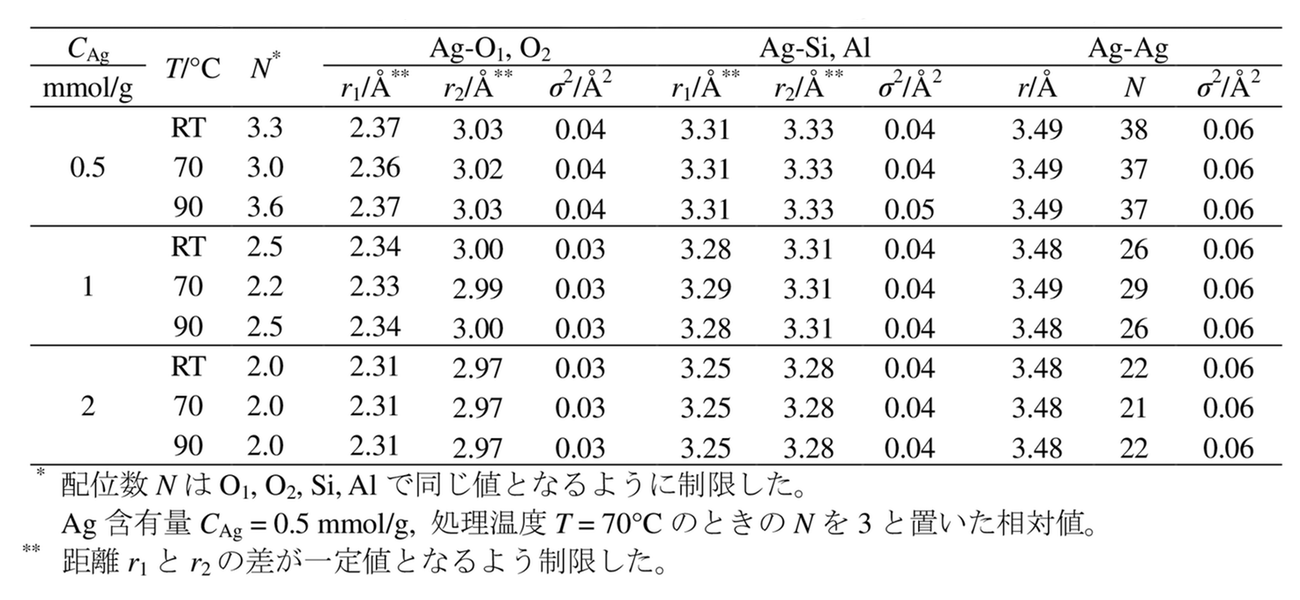
表1に水溶液中の試料のEXAFSのカーブフィッティングによる解析結果を示す。種々条件を変え解析を試行しているが未だ完全に納得の得られる条件を見出せていない。表1の結果も Ag の配位数が異常に大きいことや示していないがスケール因子も大きいことから、配位数の絶対的な値には意味はないが、相対的にその変化について考察する。また ΔE0 についても参照試料から得られる値にこれらの試料のデータにうまく適用できる値がなく、0.5 mmol/g の含有量のときの最適値を使用しているため距離の値についても確度は不明であるが、0.5 mmol/g の含有量の試料ではA型の酸素6員環中心に Ag+ があるとき[8]とほぼ同じ Ag-O 距離を示している。Ag-Ag の成分はフィッティング計算に加えた結果の最適値をあげているが、配位数が異常に大きい上に、距離はクラスター中で考えられている種々の値より明らかに長い。
表1.Ag 交換X型ゼオライトの水中での熱処理後の Ag K 吸収端EXAFS解析結果
フーリエ変換でも見られたように、すべての構造パラメータについて処理温度の違いによる変化はほとんどない。このことからも、ゼオライト中の Ag の局所構造が蛍光の強さに直接は関係していないことがわかる。含有量が増えると各原子までの距離が少しずつ短くなり、それとともに、O、Si、Al の配位数が減少していく傾向が見られる。フーリエ変換で見られた第1ピークの高さの変化は、デバイワラー因子 σ2 の減少の影響の方が大きいということになる。含有量の増加に伴うこれらの変化は、Ag+ が酸素6員環の中心からずれていくような、より対称性の高い位置から低い位置へ偏っていく変化を示唆しているように思われる。ただし、蛍光強度が最も高い含有量が 1 mmol/g のときでも明確な特徴は見られない。
今後の課題:
表1に示した値は確度がまだ低い結果であり、さらに妥当な結果が得られる解析条件を見出す必要がある。Ag 交換ゼオライトの Ag 周囲のEXAFS解析では、可能性のある散乱原子の種類が多い一方で、良好な解析に必要な χ(k)を確保することが難しく、解析は意外に容易ではない。既報の解析結果[9]でも物理的に疑問な値が散見される。積算時間をよりずっと多くするとより細かい議論ができるEXAFSが得られる可能性もあるが、χ(k)を見たところでは Ag 交換ゼオライト中の Ag では k = 8 Å-1 付近は多電子吸収のような構造にも見え、仮に多電子吸収であれば時間を増やすことはほとんど意味がない。それでも、他の方法で得られる知見も併用してさらに意味のある結果を導き出したい。一方、XANESで参考になる情報が得られない理由はほぼ明らかであるので、今後 Ag L吸収端の測定を行いたいと計画している。
今回の結果が示す最も重要な点は、Ag 交換ゼオライトの蛍光強度とその中の Ag の局所構造との関係がかなり薄いと示唆されることである。一方、本課題においてこれら以外の多様な調製条件での Ag 交換ゼオライトのX線吸収スペクトルを測定したので、強度以外の蛍光スペクトルの形状等と Ag の局所構造との関係がないか今後明らかにしたい。
参考文献:
[1] T. Sun and K. Seff, Chem. Rev., 94, 857 (1994).
[2] J. Zheng et al., Ann. Rev. Phys. Chem., 58, 409 (2007).
[3] H. Lin et al., Appl. Phys. Lett., 105, 211903 (2014).
[4] T. Miyanaga et al., Micropor. Mesopor. Mater., 168, 213 (2013).
[5] 特開2012-52102.
[6] H. Sakane et al., Jpn. J. Appl. Phys., 32, 4641 (1993).
[7] B. Ravel and M. Newville, J. Synchrotron Rad., 12, 537 (2005).
[8] A. Mayoral et al., Micropor. Mesopor. Mater., 166, 117 (2013).
[9] E. Coutino-Gonzalez et al., J. Mater. Chem. C, 3, 11857 (2015).
ⒸJASRI
(Received: March 29, 2018; Early edition: August 24, 2018; Accepted: December 17, 2018; Published: January 25, 2019)